кариокинез, непрямое деление клетки, наиболее распространённый способ воспроизведения (репродукции) клеток (См. Клетка), обеспечивающий тождественное распределение генетического материала между дочерними клетками и преемственность хромосом (См. Хромосомы) в ряду клеточных поколений. Биологическое значение М. определяется сочетанием в нём удвоения хромосом путём продольного расщепления их и равномерного распределения между дочерними клетками. Началу М. предшествует период подготовки, включающий накопление энергии, синтез дезоксирибонуклеиновой кислоты (См. Дезоксирибонуклеиновая кислота) (ДНК) и репродукцию центриолей (См. Центриоли). Источником энергии служат богатые энергией, или так называемые макроэргические, соединения. М. не сопровождается усилением дыхания, т. к. окислительные процессы происходят в интерфазе (См. Интерфаза) (наполнение «энергетического резервуара»). Периодическое наполнение и опустошение энергетического резервуара — основа энергетики М.
Стадии митоза. Единый процесс М. обычно подразделяют на 4 стадии: профазу, метафазу, анафазу и телофазу (рис. 1, 2). Иногда описывают ещё одну стадию, предшествующую началу профазы, — препрофазу (антефазу). Препрофаза — синтетическая стадия М., соответствующая концу интерфазы (S — G2 периоды), включает удвоение ДНК и синтез материала митотического аппарата (См. Митотический аппарат). В профазе происходят реорганизация ядра с конденсацией и спирализацией хромосом, разрушение ядерной оболочки и формирование митотического аппарата путём синтеза белков и «сборки» их в ориентированную систему веретена деления клетки (См. Веретено деления клетки). Метафаза заключается в движении хромосом к экваториальной плоскости (метакинез, или прометафаза), формировании экваториальной пластинки («материнской звезды») и в разъединении хроматид, или сестринских хромосом. Анафаза — стадия расхождения хромосом к полюсам. Анафазное движение связано с удлинением центральных нитей веретена, раздвигающего митотические полюсы, и с укорочением хромосомальных микротрубочек (См. Микротрубочки) митотического аппарата. Удлинение центральных нитей веретена происходит либо за счёт поляризации «запасных» макромолекул, достраивающих микротрубочки веретена, либо за счёт дегидратации этой структуры. Укорочение хромосомальных микротрубочек обеспечивается свойствами сократительных белков митотического аппарата, способных к сокращению без утолщения. Телофаза заключается в реконструкции дочерних ядер из хромосом, собравшихся у полюсов, разделении клеточного тела (цитотомия, цитокинез) и окончательном разрушении митотического аппарата с образованием промежуточного тельца. Реконструкция дочерних ядер связана с деспирализацией хромосом, восстановлением ядрышка и ядерной оболочки. Цитотомня осуществляется путём образования клеточной пластинки (в растительной клетке) или путём образования борозды деления (в животной клетке). Механизм цитотомии связывают либо с сокращением желатинизированного кольца цитоплазмы, опоясывающего экватор (гипотеза «сократимого кольца»), либо с расширением поверхности клетки вследствие распрямления петлеобразных белковых цепей (гипотеза «расширения мембран»).
Продолжительность митоза зависит от размеров клеток, их плоидности, числа ядер, а также от условий окружающей среды, в частности от температуры. В животных клетках М. длится 30—60 мин, в растительных — 2—3 часа. Более длительны стадии М., связанные с процессами синтеза (препрофаза, профаза, телофаза); самодвижение хромосом (метакинез, анафаза) осуществляется быстро.
Регуляция митоза. В организме М. контролируются системой нейрогуморальной регуляции, которая осуществляется нервной системой, гормонами надпочечников, гипофиза, щитовидной и половых желёз, а также местными факторами (продукты тканевого распада, функциональная активность клеток). Взаимодействие различных регуляторных механизмов обеспечивает как общие, так и местные изменения митотической активности. М. опухолевых клеток выходят из-под контроля нейрогуморальной регуляции.
Выражением регуляции М. в связи с взаимодействием организма и среды служит суточный ритм деления клеток. В большинстве органов ночных животных максимум М. отмечается утром, а минимум — в ночное время. У дневных животных и человека отмечается обратная динамика суточного ритма. Суточный ритм М. — следствие цепной реакции, в которую вовлекаются ритмические изменения внешней среды (освещённость, температура, режим питания и др.), ритм функциональной активности клеток и изменения процессов обмена веществ (см. Биологические ритмы).
Нарушения митоза. При различных патологических процессах нормальное течение М. нарушается. Выделяют 3 основных вида патологии М. 1) Повреждения хромосом (набухание, склеивание, фрагментация, образование мостов, повреждения центромеров, отставание отдельных хромосом при движении, нарушение их спирализации и деспирализации, раннее разъединение хроматид, образование микроядер. 2) Повреждения митотического аппарата (задержка М. в метафазе, многополюсный, моноцентрический и асимметричный М., трёхгрупповая и полая метафазы). Особое значение в этой группе патологии М. имеет колхициновый М., или К-митоз, который вызывается алкалоидом колхицином (отсюда название), а также колцемидом, винбластином, винкристином, аценафтеном и др. т. н. статмокинетическими ядами, используемыми в качестве мутагенов (См. Мутагены). К-митозы возникают и самопроизвольно в культуре ткани и опухолях. При К-митозе нарушаются расхождение центриолей и поляризация ими веретена деления, подвергается дезорганизации митотический аппарат, не происходит разъединения хроматид (К-пары). 3) Нарушения цитотомии. Патологические М. возникают после воздействия митотических ядов, токсинов, экстремальных факторов (ионизирующее излучение, аноксия, гипотермия), при вирусной инфекции и в опухоли. Резкое увеличение числа патологических М. типично для злокачественных опухолей.
Лит.: Мэзия Д., Митоз и физиология клеточного деления, пер. с англ., М., 1963; Цанев Р. Г., Марков Г. Г., Биохимия клеточного деления, пер. с болг., М., 1964; Алов И. А., Очерки физиологии митотического деления клеток, М., 1964; Епифанова О. И., Гормоны и размножение клеток, М., 1965; Алов И. А., Цитофизиология и патология митоза, М., 1972; Wassermann F., Wachstum und Vermehrung der Lebendigeii Massen, B., 1929 (Handbuch der Mikroskopischen Anatomie des Menschen, Hrsg. W. Möllendorff, 1929, Bd 1, Tl 2); Hughes A., The mitotic cycle, L., 1952; Schrader F., Mitosis, 2 ed., N. Y., 1953; Grundmann E., Der Mitotische Zeilcyclus, в кн.: Handbuch der allgemeinen Pathologie, Hrsg, H. Altman, Bd 2, Tl 1, B. — HdIb. — N. Y., 1971, S. 282—479.
И. А. Алов.
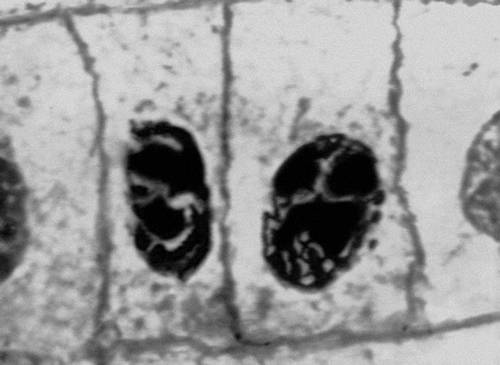
Рис. 2 (1). Митоз в меристематических клетках корешка лука (микрофотография). Интерфаза.

Рис. 2 (2). Митоз в меристематических клетках корешка лука (микрофотография). Профаза (фигура рыхлого клубка).
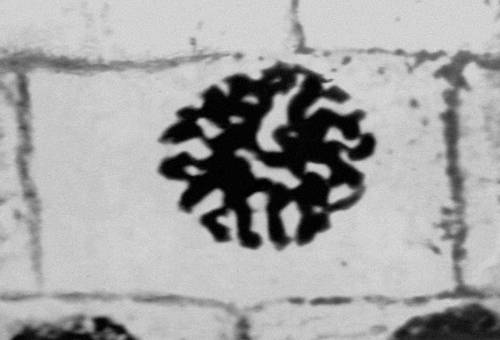
Рис. 2 (3). Митоз в меристематических клетках корешка лука (микрофотография). Поздняя профаза (разрушение ядерной оболочки).

Рис. 2 (4). Митоз в меристематических клетках корешка лука (микрофотография). Прометафаза.

Рис. 2 (5). Митоз в меристематических клетках корешка лука (микрофотография). Метафаза.
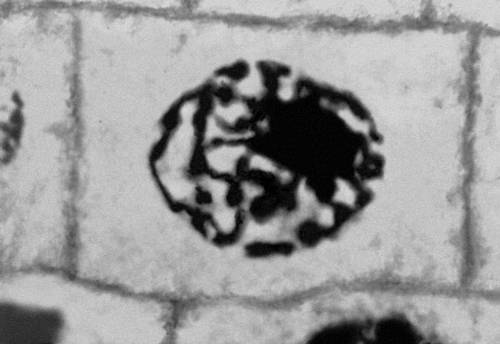
Рис. 2 (6). Митоз в меристематических клетках корешка лука (микрофотография). Анафаза.

Рис. 2 (7). Митоз в меристематических клетках корешка лука (микрофотография). Ранняя телофаза.

Рис. 2 (8). Митоз в меристематических клетках корешка лука (микрофотография). Поздняя телофаза.
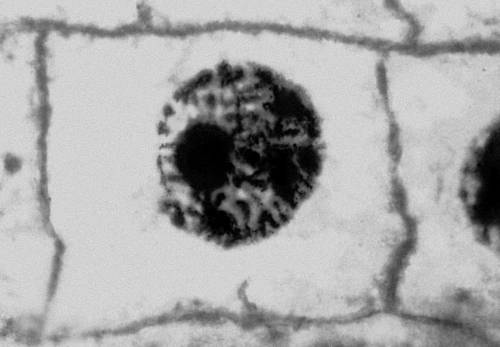
Рис. 2 (9). Митоз в меристематических клетках корешка лука (микрофотография). Образование дочерних клеток.

Рис. 1. Схема митоза: 1, 2 — профаза; 3 — прометафаза; 4 — метафаза; 5 — анафаза; 6 — ранняя телофаза; 7 — поздняя телофаза.
Большая советская энциклопедия. — М.: Советская энциклопедия. 1969—1978.