- РЕНТГЕНОЭЛЕКТРОННАЯ СПЕКТРОСКОПИЯ
-
(электронная спектроскопиядля химического анализа) (РЭС, ЭСХА) - совокупность методов определениястроения хим. соединений, состава и структуры поверхности твёрдых тел наоснове анализа фотоэлектронов, вылетающих из вещества под воздействиемрентг. излучения.
Кинетич. энергия фотоэлектронов
 , выбитых рентг. квантом hv (v - частота рентг. излучения) с внутр. или внеш. оболочек атома, равна
, выбитых рентг. квантом hv (v - частота рентг. излучения) с внутр. или внеш. оболочек атома, равна 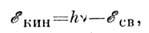
где
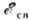 - энергия связи электрона в образце, определяемая энергией электрона ватоме и взаимодействиями атома с др. атомами (хим. связью в молекуле ивзаимодействием с атомами др. молекул). Т. о., анализ кинетич. энергиивылетающих из вещества электронов позволяет получить информацию об элементномсоставе образца, распределении хим. элементов по поверхности твёрдого тела, характере хим. связей и др. взаимодействий атомов образца.
- энергия связи электрона в образце, определяемая энергией электрона ватоме и взаимодействиями атома с др. атомами (хим. связью в молекуле ивзаимодействием с атомами др. молекул). Т. о., анализ кинетич. энергиивылетающих из вещества электронов позволяет получить информацию об элементномсоставе образца, распределении хим. элементов по поверхности твёрдого тела, характере хим. связей и др. взаимодействий атомов образца.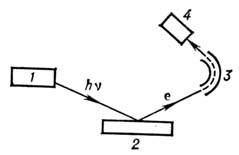
Рис. 1. Схема электронного спектрометра: 1 - источник излучения;2 - образец; 3 - электронный энергоанализатор; 4 - детектор.
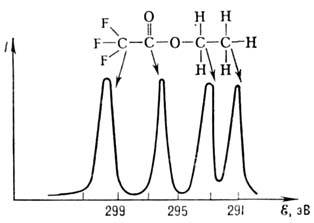
Рис. 2. Рентгеноэлектронный спектр С 1s этилтрифторацетата.
В электронных спектрометрах (рис. 1), используемых в Р. с., на образецвоздействуют излучением рентг. трубки (обычно линии .
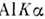 пли
пли 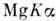 сэнергиями квантов соотв. 1486 и 1254 эВ) или рентг. синхротронным излучением. Выбитые электроны попадают в электронный энергоанализатор, к-рый разделяетих по
сэнергиями квантов соотв. 1486 и 1254 эВ) или рентг. синхротронным излучением. Выбитые электроны попадают в электронный энергоанализатор, к-рый разделяетих по  Монохроматич. пучки электронов попадают в детектор, измеряющий интенсивность пучков. Т. о. получают рентгеноэлектронный спектр - распределение рентг. фотоэлектроновпо их кинетич. энергиям, максимумы в нём - спектральные линии - отвечаютопредел. атомам (рис. 2); максимумы иногда сливаются. Отд. линии обозначаютсимволом элемента, рядом с к-рым указывают уровень энергии фотоэлектрона(напр., линия С 1s означает: электроны вылетают с уровня 1s углерода).
Монохроматич. пучки электронов попадают в детектор, измеряющий интенсивность пучков. Т. о. получают рентгеноэлектронный спектр - распределение рентг. фотоэлектроновпо их кинетич. энергиям, максимумы в нём - спектральные линии - отвечаютопредел. атомам (рис. 2); максимумы иногда сливаются. Отд. линии обозначаютсимволом элемента, рядом с к-рым указывают уровень энергии фотоэлектрона(напр., линия С 1s означает: электроны вылетают с уровня 1s углерода).Р. с. позволяет исследовать все элементы (кроме Н) при содержании ихв образце ~10-5 г (пределы обнаружения элемента с помощью РЭС10-7 - 10-9 г). Относит. содержание элемента можетсоставлять доли процента. Образцы могут быть твёрдыми, жидкими или газообразными.
Величина
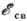 электрона внутр. оболочки атома А в хим. соединении определяется эфф. зарядомZA этого атома и электростатич. потенциалом U, создаваемымвсеми др. атомами соединения:
электрона внутр. оболочки атома А в хим. соединении определяется эфф. зарядомZA этого атома и электростатич. потенциалом U, создаваемымвсеми др. атомами соединения: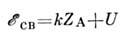
(k - коэф. пропорциональности). Значение
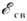 сравнивают с энергией связи аналогичного электрона в стандартном веществе(кристаллич. модификации данного элемента) и вводят понятие хим. сдвига
сравнивают с энергией связи аналогичного электрона в стандартном веществе(кристаллич. модификации данного элемента) и вводят понятие хим. сдвига 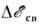 Знак
Знак 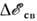 определяет знак эфф. заряда ZA атома А в хим. соединениях;значение
определяет знак эфф. заряда ZA атома А в хим. соединениях;значение 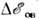 пропорционально ZA. Поскольку эфф. заряд ZA зависитот степени окисления атома А, характера соседних атомов и геом. структурысоединения, по
пропорционально ZA. Поскольку эфф. заряд ZA зависитот степени окисления атома А, характера соседних атомов и геом. структурысоединения, по 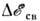 можно также определять природу функциональных групп, степень окисленияатома, способ координации лигандов н т. д.
можно также определять природу функциональных групп, степень окисленияатома, способ координации лигандов н т. д.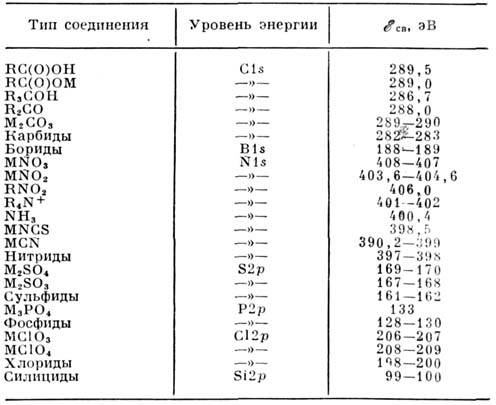
Энергии связи электронов атомов функциональных групп практически независят от типа хим. соединения, в к-ром находится данная функциональнаягруппа. В табл. приведены значения
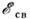 для нек-рых функциональных групп и лигандов. Относит. интенсивность максимумов, соответствующих разл. функциональным группам (или лигандам), пропорциональначислу таких групп в соединении. Напр., в Na2[Fe(CN)5NO]интенсивность линии N1s групп CN в 5 раз выше, чем линии N1s группы NO.что может быть использовано Энергии связи электронов центрального атомав некоторых функциональных группах и лигандах для определения числа разл. функциональных групп (лигандов) в соединении. Значения
для нек-рых функциональных групп и лигандов. Относит. интенсивность максимумов, соответствующих разл. функциональным группам (или лигандам), пропорциональначислу таких групп в соединении. Напр., в Na2[Fe(CN)5NO]интенсивность линии N1s групп CN в 5 раз выше, чем линии N1s группы NO.что может быть использовано Энергии связи электронов центрального атомав некоторых функциональных группах и лигандах для определения числа разл. функциональных групп (лигандов) в соединении. Значения 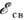 в самом лиганде закономерно зависит от особенностей хим. соединения; напр.,в случае аниона
в самом лиганде закономерно зависит от особенностей хим. соединения; напр.,в случае аниона 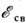 его внутр. электронов растёт с увеличением электроотрицательности связанногос ним катиона. Хим. сдвиг
его внутр. электронов растёт с увеличением электроотрицательности связанногос ним катиона. Хим. сдвиг 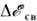 увеличивается с ростом степени окисления атома.
увеличивается с ростом степени окисления атома.Увеличение (уменьшение)
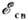 электронов внутр. оболочек соответствует уменьшению (увеличению) электроннойплотности на рассматриваемом атоме. Так, следует ожидать повышения энергиисвязи электронов в атомах-донорах, поскольку электронная плотность донорасмещается к атомам координац. сферы, атомы-акцепторы, напротив, принимаютчасть электронной плотности от центр. атома, вследствие чего
электронов внутр. оболочек соответствует уменьшению (увеличению) электроннойплотности на рассматриваемом атоме. Так, следует ожидать повышения энергиисвязи электронов в атомах-донорах, поскольку электронная плотность донорасмещается к атомам координац. сферы, атомы-акцепторы, напротив, принимаютчасть электронной плотности от центр. атома, вследствие чего 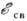 его электронов уменьшается.
его электронов уменьшается.Р. с.- один из осн. методов определения состава поверхности, он широкоиспользуется при изучении адсорбции, катализа, коррозии и т. д. ПрименениеРЭС для этих целей основано на прямой зависимости интенсивности I А линий изучаемых атомов А от их концентрации С А в поверхностномслое толщиной 2-3 нм, сопоставимой с длиной свободного пробега
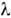 электрона в веществе без взаимодействия с др. электронами:
электрона в веществе без взаимодействия с др. электронами: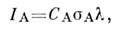
где
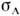 - сечение фотоионизации с соответствующего уровня энергии, определяющеевероятность ионизации этого уровня в атоме А. Для уровня энергии i атомовА н уровня k атомов В справедливо соотношение:
- сечение фотоионизации с соответствующего уровня энергии, определяющеевероятность ионизации этого уровня в атоме А. Для уровня энергии i атомовА н уровня k атомов В справедливо соотношение: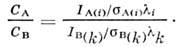
Величины
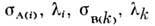 можно рассчитать теоретически и на основе измеренных значений
можно рассчитать теоретически и на основе измеренных значений 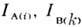 определить С A/С В. Надёжнее, однако, измеритьотношение
определить С A/С В. Надёжнее, однако, измеритьотношение 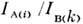 для нескольких известных значений С A/С В иэкспериментально определить величину пост. множителя
для нескольких известных значений С A/С В иэкспериментально определить величину пост. множителя 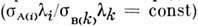 ,а затем определять отношение концентраций по измеренным значениям
,а затем определять отношение концентраций по измеренным значениям 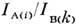 ). Этот приём наз. методом градуировочных кривых.
). Этот приём наз. методом градуировочных кривых.Методами РЭС можно установить распределение концентрации элемента поглубине образца, для чего применяют, напр., травление поверхности пучкамиионов Аr+, Кr+. С их помощью в течение 1 мин с поверхностиобразца удаляется слой толщиной до неск. десятков нм. Через определ. промежуткивремени проводят рентгеноэлектронный анализ поверхности и получают зависимостьинтенсивностей определ. линий от времени травления (или от глубины, еслиизвестна скорость травления). Т. о. можно проводить послойный анализ наглубину до неск. мкм. Используя зависимость интенсивности линий фотоэлектронногоспектра от угла
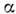 ,определяют изменения состава образца по глубине до 10 нм без его разрушения.
,определяют изменения состава образца по глубине до 10 нм без его разрушения.Р. с.- единств. метод, позволяющий определить толщину d и качествомонокристаллич. плёнок толщиной 0,5-3,0 нм. Метод основан на экспоненц. зависимости I от d и
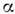 :
: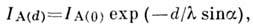 где
где 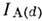 и
и 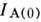 - интенсивности линий элемента А соответственно при наличии на подложкеплёнки толщиной d и без неё;
- интенсивности линий элемента А соответственно при наличии на подложкеплёнки толщиной d и без неё;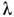 - длина свободного пробега фотоэлектронов в плёнке. Для расчёта d достаточноизмерить
- длина свободного пробега фотоэлектронов в плёнке. Для расчёта d достаточноизмерить 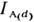 при двух разл. значениях угла
при двух разл. значениях угла 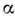
Вследствие дифракции фотоэлектронов адсорбиров. молекулы на атомах адсорбента-монокристаллаинтенсивность рентгеноэлектронного спектра зависит от углов между потокомфотоэлектронов и разл. направлениями в монокристалле. Эта зависимость позволяетопределить способ координации адсорбиров. молекулы.
Лит.: Немошкаленко В. В., Алешин В. Г., Электронная спектроскопиякристаллов, 2 изд., К., 1983; Миначев X. М., Антошин Г. В., Шпиро Е. С.,Фотоэлектронная спектроскопия и ее применение в катализе, М., 1981; НефедовВ. И., Ч е р е п и н В. Т., Физические методы исследования поверхноститвердых тел, М., 1983; Н е ф е д о в В. И., Рентгеноэлектронная спектроскопияхимических соединений, М., 1984. В. И. Нефедов.
Физическая энциклопедия. В 5-ти томах. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1988.
.