TITANE
Le titane est l’élément chimique de symbole Ti, de numéro atomique 22 et de poids atomique 48. Il appartient au groupe IVb de la classification périodique. Il fut découvert par W. Gregor en 1791 et dénommé par M. H. Klaproth en 1795.
C’est le neuvième élément par ordre d’abondance dans la croûte terrestre, et la plupart des roches éruptives ou sédimentaires en contiennent. La première utilisation industrielle semble être un additif, parfois en quantité notable, aux fontes et aciers sous forme de ferrotitane au début de ce siècle. Ce métal fut une curiosité de laboratoire jusqu’en 1936, date à laquelle W. Kroll montra que le titane ductile pouvait être produit industriellement par réduction de tétrachlorure de titane par le magnésium.
C’est un métal blanc à l’éclat métallique qui présente une densité égale à 4,5, une résistance mécanique assez faible associée à une grande ductilité et une bonne résistance à la corrosion. Ses caractéristiques mécaniques sont fortement augmentées par l’addition d’éléments d’alliages.
Le titane est utilisé principalement comme élément d’addition aux alliages métalliques, à l’état pur, sous forme d’alliages à base de titane ou sous forme de composés: oxyde (blanc de titane) et carbure.
La production du métal, sans cesse croissante depuis 1950, est en baisse depuis 1990, car la demande mondiale d’éponges de titane dans l’industrie a diminué.
Production du titane
Minerais
Le titane est présent en quantité notable dans les minéraux suivants: rutile (TiO2), ilménite (FeO 練 Ti2), arizonite (Fe2Ti39), perovskite (CaTiO3), sphène (CaTiSiO5), par exemple. Certains minerais de fer sont titanifères (taux de titane inférieur à 40 p. 100). Seuls le rutile et l’ilménite, titrant respectivement 90 p. 100 (et plus) et de 40 à 60 p. 100 d’oxyde Ti2, sont utilisés industriellement comme sources de titane, et seul le rutile a été employé dans la production du titane à l’état métallique. Cependant, des recherches se poursuivent pour transformer l’ilménite plus abondante en «rutile artificiel» (procédé Sorel au Canada, procédé Osaka au Japon). La production d’ilménite dans le monde a dépassé 3 500 000 t en 1992, les principaux producteurs étant l’Australie (915 000 t), le Canada (500 000 t), en 1984, la Norvège et l’U.R.S.S. étaient également des gros producteurs. La production mondiale de rutile a dépassé 400 000 t par an en 1992, les principaux pays producteurs étant l’Australie (180 000 t), la Sierra Leone, les États-Unis.
Métallurgie extractive
Les principales étapes de la métallurgie extractive classique sont les suivantes:
– concentration des minerais;
– chloration en présence de coke vers 800 0C-1 000 0C:

– condensation du tétrachlorure TiCl4, purification par voie chimique et distillation fractionnée;
– réduction du tétrachlorure par le magnésium (ou le sodium) vers 800 0C en atmosphère d’argon:
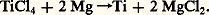
Le titane est obtenu sous forme poreuse (éponge) dont l’excès de chlorure de magnésium est distillé sous vide vers 900 0C-1 000 0C ou lixivié par lavage acide.
Consolidation de l’éponge
L’éponge de titane est consolidée par fusion en four à arc sous vide (ou sous argon) avec électrode consommable ou non consommable, ce qui permet de produire des lingots ou des pièces moulées.
À partir de ce stade, les opérations de transformation à chaud et à froid se font sur des équipements classiques, avec cependant certaines précautions spécifiques, notamment en ce qui concerne l’atmosphère des fours.
Production mondiale
La production mondiale d’éponge de titane est assurée principalement par trois pays dont les tonnages en 1992 étaient approximativement les suivants: l’ex-U.R.S.S. 20 000 t par an, le Japon 16 000 t par an et les États-Unis 11 000 t par an, puis la Grande-Bretagne et la Chine.
Le titane métallique
Propriétés physiques
Les principales propriétés physiques du titane sont les suivantes:
– point de fusion: 1 680 0C;
– module de Young: 11 000 憐 105 hPa;
– résistivité électrique: 50 猪行 練 cm à 20 0C;
– chaleur spécifique: 544 joules 練 kg-1 練 0C-1 à 20 0C;
– coefficient de dilatation: 8,5 練 10-6 練 0C-1 à 20 0C;
– amagnétisme.
Caractéristiques mécaniques
Les caractéristiques mécaniques du titane varient avec la teneur en impuretés résiduelles, et la charge de rupture à l’ambiante du titane non allié (ou commercialement pur) varie de 35 憐 105 à 70 憐 105 hPa. Le métal présente une grande ductilité et ne se fragilise pas aux basses températures. Il peut subir toutes les opérations mécaniques (laminage, filage, étirage). C’est un excellent métal structural plus léger que les aciers, mais son prix est encore relativement élevé.
Résistance à la corrosion
Le titane résiste à la corrosion dans de nombreux environnements comprenant les milieux naturels (eau de mer, atmosphère, liquides physiologiques, par exemple) et de nombreux milieux chimiques parmi lesquels on peut citer les chlorures en solution relativement neutre, l’acide nitrique, le chlore humide, les acides «oxydants». En revanche, il résiste mal aux acides réducteurs (H2S4, HCl, H3P4, entre autres), à certains composés fortement oxydants (Cl2 sec, H3 fumant rouge, H22, par exemple), aux composés fluorés ionisables, aux solutions alcalines chaudes et à certains métaux liquides. La résistance à la corrosion du titane est fortement élargie par l’addition de 0,2 p. 100 de palladium, de 1,5 p. 100 de nickel, ou de molybdène jusqu’à 30 p. 100 en poids.
Ses principales applications dans ce domaine sont: l’industrie du chlore et de la soude, le blanchiment de la pâte à papier et des textiles, la production d’engrais, la chimie de synthèse organique (acétaldéhyde, acide téréphtalique, urée), la galvanoplastie, les industries pétrochimiques, l’utilisation de l’eau de mer (condenseurs des centrales thermiques, dessalement).
Ce secteur représente environ 10 p. 100 des usages du titane aux États-Unis et environ 30 p. 100 en Europe occidentale.
Alliages de titane
Le titane solide possède deux structures cristallines: hexagonale compacte (phase 見) au-dessous de 880 0C et cubique centrée (phase 廓) au-delà. Ce dimorphisme est à la base de la classification pratique des alliages de titane et de leur possibilité de traitement thermique. On distingue, suivant la nature et la quantité d’éléments d’alliages, les familles «alpha », «alpha-bêta » et «bêta » ayant chacune des propriétés d’usage particulières. Les plus hautes résistances mécaniques sont obtenues avec les alliages 廓 (jusqu’à 145 憐 105 Pa), ce qui, étant donné leur densité, correspond à un indice résistance/masse volumique parmi les plus élevés (face=F0019 力 3 000 hPa 練 kg-1 練 m3).
Les alliages de titane sont donc utilisés pour l’essentiel dans l’industrie aéronautique et spatiale, soit dans les moteurs à réaction (compresseurs), soit dans la cellule ou les trains d’atterrissage, dans les hélicoptères (moyeu-rotor), dans les engins spatiaux (capsules et fusées). Ils trouvent des emplois, actuellement secondaires, dans la construction navale et automobile, l’armement, les industries du vide, par exemple. Les compositions et caractéristiques types à l’ambiante de quelques alliages courants de titane sont données dans le tableau ci-dessous.
Composés du titane
La plus large part du titane consommé dans le monde (plus de 90 p. 100) l’est sous forme combinée. Les deux composés les plus importants sont l’oxyde et le carbure.
Oxyde
L’oxyde est utilisé principalement (à 75 p. 100) comme pigment pour les peintures, laques et émaux et charges de papier, sous le nom de blanc de titane, en raison de qualités spécifiques exceptionnelles: indice de réfraction, pouvoir couvrant, éclat, prise d’huile, pouvoir tinctorial. Il est généralement produit à partir de l’ilménite par le procédé dit au sulfate ou par oxydation du chlorure (à partir du rutile). Le reste est utilisé comme revêtement d’électrodes de soudage, constituant de céramiques et réfractaires, de revêtement de sols, caoutchouc, encre d’imprimerie, etc. La production mondiale d’oxyde Ti2 était de l’ordre de 1,8 million de tonnes en 1970 et approchait 3 millions de tonnes à la fin de cette décennie.
Carbure
Le carbure TiC est un composé réfractaire, d’une grande dureté (2 470 knoops), au point de fusion très élevé (face=F0019 力 3 260 0C), de faible densité (4,93); il entre dans la constitution d’outils coupants (en concurrence avec le carbure de tungstène), d’abrasifs et de matériaux réfractaires.
Élément d’addition aux alliages métalliques
Le titane est utilisé comme additif aux alliages métalliques tels que les aciers, les alliages légers et cuivreux, le molybdène, les superalliages à base de nickel, les aimants permanents, par exemple. Il agit soit comme désoxydant, décarburant et dénitrurant ou inoculant (faibles additions), soit comme élément d’alliage (fortes additions). Il est introduit dans les aciers sous forme de ferro-titane , de divers titres (25, 40 et 70 p. 100), préparés par métallothermie ou au four à induction. La production de ferrotitane utilisé dans l’industrie pétrolière n’est pas en expansion.
titane [ titan ] n. m.
• 1803; lat. mod. titanium (1795); de Titan, d'apr. uranium
♦ Chim. Élément atomique (Ti; no at. 22; m. at. 47,90), métal blanc brillant utilisé en alliages. Blanc de titane : oxyde utilisé en peinture.
● titane nom masculin (latin scientifique titanium, du grec titanos, chaux) Métal habituellement tétravalent, dont les propriétés rappellent celles du silicium et de l'étain. (Élément chimique de symbole Ti.) Numéro atomique : 22 Masse atomique : 47,90 Point de fusion : 1 660 °C Masse volumique : 4,54 g°cm3
titane
n. m. CHIM élément métallique (symbole Ti) de numéro atomique Z = 22.
— Métal (Ti).
|| Blanc de titane: dioxyde de titane, utilisé en peinture.
⇒TITANE, subst. masc.
CHIM. Corps simple, métal blanc, malléable, résistant à l'oxydation et aux acides, donnant des alliages très durs utilisés dans l'industrie, notamment pour la fabrication d'objets de précision et pour le revêtement de pièces légères en aéronautique et aérospatiale (symb. Ti, n° atomique 22, poids atomique 47,9). Sulfate, oxyde, minerai de titane. Parmi les 19 corps simples trouvés dans les émanations des volcans actuels on trouve, sauf le magnésium, le titane et le fluor, tous les corps simples qui entrent dans la composition des roches volcaniques actuelles (ÉLIE DE BEAUMONT ds B. Sté géol. Fr., t. 4, 1847, p. 8). Dans les revêtements des fours métallurgiques, on observe la diffusion d'une partie de la matière du laitier silicaté fondu et la diffusion en sens inverse du titane, du fer, du manganèse et de la chaux du revêtement (FURON ds R. gén. sc., t. 63, 1956, p. 40).
♦ Blanc de titane. Anhydride titanique utilisé comme pigment blanc pour la peinture, l'émail, le papier. Le blanc de titane, qui n'est pas vénéneux, qui est très résistant, couvre bien, moins toutefois que le plomb (OVIO, Vision coul., 1932, p. 141). L'architecte André Lurçat a également imaginé des murs réflecteurs paraboliques au blanc de titane (BENOIST, Musées, 1960, p. 60).
REM. 1. Titanique, adj., chim. [En parlant d'un composé] Qui renferme du titane trivalent. Synon. blanc de titane (supra). Anhydride titanique; magnétite titanique. Cette espèce, qui peut renfermer des parties égales des deux oxydes ferrique ou titanique, cristallise en rhomboèdres (LAPPARENT, Minér., 1899, p. 566). Le seul minerai important d'aluminium est la bauxite, découverte dans le curieux pays des Baux (Vaucluse). C'est un hydrate d'alumine qui renferme de l'oxyde de fer, de la silice et de l'acide titanique (GUILLET, Techn. métall., 1944, p. 77). 2. Titanisation, subst. fém., chim. Action du titane ou d'un composé du titane sur la surface d'un objet; traitement au titane. La titanisation du verre est pratiquée sur des bouteilles et des flacons, après démoulage et avant recuisson (Lar. encyclop. Suppl. 1975). 3. Titaniser, verbe trans., chim. Faire subir la titanisation à quelque chose. Part. passé adj. Les bouteilles titanisées ont des propriétés analogues à celles sur lesquelles on a déposé de l'oxyde d'étain (Lar. encyclop. Suppl. 1975). 4. Titan(o)-, (Titan-, Titano-)élém. formant entrant dans la constr. de termes sav. en chim. et minér., désignant des composés du titane ou des phénomènes de combinaison du titane. a) Titanifère, adj. Qui contient du titane. Synon. titané (infra dér. 2). Filon titanifère. Toutes les roches volcaniques contiennent au contraire, généralement, du fer oxidulé [oxydulé] titanifère qu'on peut considérer comme un reste de base (ÉLIE DE BEAUMONT ds B. Sté géol. Fr., t. 4, 1847, p. 4). Certaines variétés d'oligiste sont titanifères et préparent la transition à une espèce isomorphe, qui est (...) [le] fer titané (LAPPARENT, Minér., 1899, p. 566). b) Titanoniobate, titano-niobate (-niobate, du rad. de niobium + -ate), subst. masc. Sel composé de titane et d'un sel de niobium. Titanoniobate d'yttrium, de thorium. Titano-niobate de chaux, en petits cubes d'un noir de fer (LAPPARENT, Minér., 1899, p. 537). c) Titanosilicate, subst. masc. Combinaison de silice et de titane. Dans des conditions analogues on trouve parfois des concentrations de quelques autres minéraux manganifères (...), des spinelles, des titanosilicates (VERNADSKY, Géochim., 1924, p. 76). d) Titanoxyde, subst. masc. Synon. de rutile. Genre titanoxyde. Rutile (...). Macles fréquentes (LAPPARENT, Minér., 1899, p. 505). e) Titano-zirconate, subst. masc. Combinaison de titane et de zircon. Un titano-zirconate de fer et de chaux (LAPPARENT, Minér., 1899, p. 538).
Prononc.:[titan]. Homon. titane (fém. de titan). Étymol. et Hist. 1800 (ds Ann. chim., t. 34, p. 270). Terme sc., dér. sav. du lat. Titan, gr.  , v. titan, d'abord sous la forme titanium, cf. attest. 1798 s.v. tellure d'apr. uranium, créé par le chimiste all. Klaproth, v. tellure, ca 1795 (cf. Brockhaus Enzykl., s.v. titan), v. aussi NYSTEN 1824.
, v. titan, d'abord sous la forme titanium, cf. attest. 1798 s.v. tellure d'apr. uranium, créé par le chimiste all. Klaproth, v. tellure, ca 1795 (cf. Brockhaus Enzykl., s.v. titan), v. aussi NYSTEN 1824.
 , v. titan, d'abord sous la forme titanium, cf. attest. 1798 s.v. tellure d'apr. uranium, créé par le chimiste all. Klaproth, v. tellure, ca 1795 (cf. Brockhaus Enzykl., s.v. titan), v. aussi NYSTEN 1824.
, v. titan, d'abord sous la forme titanium, cf. attest. 1798 s.v. tellure d'apr. uranium, créé par le chimiste all. Klaproth, v. tellure, ca 1795 (cf. Brockhaus Enzykl., s.v. titan), v. aussi NYSTEN 1824.DÉR. 1. Titanate, subst. masc., chim. [N. générique des sels complexes de titane, produit par la combinaison d'une base et de l'acide titanique] Titanate de sodium, de nickel, de plomb, de magnésium, de calcium. On découvre chaque année de nouveaux carbonates, silicates simples et complexes, manganites simples et complexes, ferrites, phosphates, arséniates, niobates, titanates (VERNADSKY, Géochim., 1924, p. 107). Enfin, exceptionnellement, pour les solides ferroélectriques dont le type est le titanate de baryum, elle peut dépasser 1 000 [kilovolts pour 1 cm d'épaisseur] (FRÜHLING, Cours d'électr., t. 1, 1966, p. 112). — [titanat]. — 1re attest. 1836 (Ac. Suppl.); de titane, suff. -ate. 2. Titané, -ée, adj., chim. Qui contient du titane. Le titane se trouve dans une foule de roches: c'est un des corps simples les plus répandus (...); mais il se trouve dans les roches volcaniques à l'état de fer titané seulement (ÉLIE DE BEAUMONT ds B. Sté géol. Fr., t. 4, 1847, p. 44). V. infra ex. de Wurtz. — [titane]. — 1re attest. 1842 (Ac. Compl.); de titane, suff. -é. 3. Titanite, subst. fém., minér. Silicate de calcium et de titane de couleur jaune vert, qui cristallise dans le système monoclinique. Synon. sphène. Les principaux minéraux renfermant du titane sont (...) les différentes variétés de fer titané: le sphène ou titanite (WURTZ, Dict. chim., t. 3, 1878, p. 424). Les spécimens sombres sont opaques, rouges-bruns, et portent le nom mythologique de titanite en raison du métal titane qui entre dans la composition de ce silicate (METTA, Pierres préc., 1960, p. 95). — [titanit]. — 1res attest. 1803 minér. subst. masc. (BOISTE: Titanite, schorl rouge ou sagénite), 1824 subst. fém. « titane oxydé » (Ac. Suppl.), 1964 chim. subst. masc. (Lar. encyclop.), v. aussi BRIAND-POIROT Pierres préc. 1985: ,,Titanite ou sphène [...] « sphène »``, terme exclusivement fr., de sphên « coin à fendre », fait allusion à la forme des cristaux (R.-J. HAÜY, Traité de minér., Paris, Louis, t. 1, 1801), titanite fait allusion à la composition chim. (KLAPROTH, 1795); de titane, suff. -ite, ou empr. à l'all. titanit 1795, KLAPROTH ds NED, dér. de titan-ium, v. titane, suff. -it, corresp. au fr. -ite parce que cet élément contient du titane.
titane [titan] n. m.
ÉTYM. 1803; lat. mod. titanium, 1795, Klaproth; de Titan, d'après uranium.
❖
♦ Chim. Élément (masse at. 47,90; no at. 22; symb. Ti); métal blanc brillant (dens. 4,5; température de fusion 1 675 °C), qui se rencontre dans la plupart des roches ignées ou sédimentaires et dont les principaux minerais sont le rutile et l'ilménite (titanate de fer). || Le titane est employé en métallurgie pour accroître la résistance mécanique des aciers. || L'oxyde de titane est utilisé en peinture comme pigment (blanc de titane).
❖
DÉR. Titanate, titané, 2. titanique, titanisation, titaniser, titanite
COMP. Titanifère, titanomagnétite, titanyle.
Encyclopédie Universelle. 2012.