CUIVRE
Parce qu’il existe, comme l’or et l’argent, à l’état natif, le cuivre est l’un des métaux les plus anciennement connus. Des objets de cuivre datant du neuvième millénaire avant J.-C. ont été mis au jour en Irak. Sa métallurgie semble dater du cinquième millénaire, et on peut parler d’un âge du cuivre antérieur à l’âge du bronze.
Le cuivre est aujourd’hui, par les tonnages extraits, mis en œuvre et consommés, le deuxième en importance des métaux non ferreux. L’aluminium l’a dépassé en 1964, et l’écart entre eux est sans doute appelé à croître sans cesse. En revanche, toujours en tonnage, le cuivre arrive bien avant le zinc, le plomb, le nickel et l’étain.
Si le cuivre pur – parfois encore improprement appelé «cuivre rouge» – est pour une grande part employé sans addition d’éléments d’alliage, il ne faut cependant pas négliger ceux-ci. De nombreux pays ne publiant pas de statistiques, il est difficile de fournir des chiffres précis. Cependant, on peut estimer à près de la moitié du total le tonnage consommé sous forme d’alliages. Le plus important d’entre eux est le laiton, alliage de cuivre et de zinc. Connus du grand public sous le nom (impropre) de «cuivre jaune», les laitons constituent une famille d’alliages aux propriétés et emplois très diversifiés. Viennent ensuite les bronzes, alliages de cuivre et d’étain, avec ou sans addition d’autres métaux dont les plus courants sont le zinc et le plomb. Puis viennent les cupro-aluminiums, les cupronickels, les cuprosiliciums, les cuprochromes, les cuprobérylliums...; en tout, plusieurs centaines d’alliages différents.
Pendant des siècles, le cuivre et ses alliages ont été employés pour leurs propriétés de résistance à la corrosion et de malléabilité: ustensiles, armes, outils primitifs ont été de bronze avant d’être de fer. L’aspect doré du métal et, surtout, de ses alliages les ont également fait employer en décoration. Il a fallu cependant l’avènement de l’électricité et de l’industrie moderne pour que l’on assiste à un développement considérable de l’utilisation du cuivre. On a calculé que le métal extrait depuis la préhistoire jusqu’à 1800 représentait un million de tonnes environ, soit un mois de la consommation actuelle.
Les propriétés déterminant les emplois du cuivre et de ses alliages sont, par ordre d’importance: la conductivité électrique, la résistance à la corrosion, la conductivité thermique, la malléabilité, l’aptitude au soudage et au brasage, les propriétés fongicides.
Contrairement à l’aluminium, par exemple, le cuivre n’est guère un métal structural. On conçoit mal un pont roulant, une carrosserie de camion, une cellule d’avion en cuivre. En revanche, on utilisera le cuivre et ses alliages en fonction de telle ou telle des propriétés sus énoncées, et les grandes applications du métal sont donc: la production, la transformation, le transport et l’utilisation de l’électricité sous toutes ses formes; les canalisations d’eau et de gaz; toutes les pièces, industrielles ou non, devant résister à la corrosion (hélices de bateaux, toitures de bâtiments, quincaillerie...).
Lorsqu’on étudie de plus près les emplois du cuivre et de ses alliages, on est frappé par leur diversité. Le cuivre est moins qu’autrefois un métal «apparent». Il se «cache» dans d’innombrables machines et appareils électriques. Du train à grande vitesse au puissant alternateur, de l’ordinateur à la minuscule montre de dame, de l’avion au lanceur spatial, le cuivre est présent et indispensable.
1. Métallurgie
Mines et minerais
Le cuivre est assez irrégulièrement réparti à la surface du globe. On trouve les grands gisements au sud du Bouclier canadien, dans le Michigan et le Montana, ainsi que dans le sud-ouest des États-Unis, au nord du Mexique, dans les Andes occidentales, Pérou et Chili (Chuquicamata et El Teniente), sur la plate-forme africaine (Zaïre et Zambie), en Afrique du Sud (Transvaal) et en Australie, à l’intérieur du Queensland, en Asie (Chine, Papouasie-Nouvelle-Guinée, Philippines, Indonésie), dans la C.E.I., en Pologne. Il existe de nombreuses autres mines un peu partout dans le monde, mais aucune n’est aussi importante que les précédentes. Citons: l’ex-Yougoslavie, les pays scandinaves, la Turquie, le Japon. Des indices apparaissent dans de nombreuses autres régions, mais les gisements ne sont pas toujours économiquement exploitables.
La teneur des minerais exploités varie de 0,5 à 6 p. 100, valeurs extrêmes. En pratique, un minerai contenant au moins 1,8 p. 100 de cuivre est considéré comme riche, comme pauvre au-dessous de 1 p. 100. Ces limites varient cependant suivant les conditions locales: profondeur, possibilités d’exploiter à ciel ouvert, frais de transport, main-d’œuvre.
Les minerais rencontrés sont très divers; on en distingue plus de 165 variétés, dont les principales sont: les métaux sulfurés primaires (chalcopyrite CuFeS2 et bornite Cu5FeS4); les minéraux oxydés secondaires [malachite CuC3,Cu(OH)2, souvent associée à l’azurite 2 CuC3,Cu(OH)2]; les minéraux sulfurés secondaires, qui sont des minerais sulfurés dissous par les eaux et redéposés.
En pratique, la plupart des gisements exploitables contiennent des métaux associés tels que le fer, le nickel, le zinc ou le plomb, et parfois des métaux tels que le cobalt, le molybdène ou le germanium, et des éléments non métalliques comme le sélénium et le tellure. L’or, l’argent, le platine et ses métaux annexes se rencontrent également souvent dans les minerais de cuivre.
Sulfurés ou oxydés, les minerais ne peuvent être réduits directement à cause de leur faible teneur. On doit donc concentrer au préalable la partie utile. Cette opération sépare les roches stériles des sulfures ou oxydes, augmente la teneur en cuivre de la partie à traiter ultérieurement et sépare, le cas échéant, les sulfures des différents métaux (zinc ou nickel, par exemple).
Il ne faut pas imaginer les minerais de cuivre comme de gros blocs tels que ceux que l’on admire dans les collections minéralogiques. Les particules cuprifères dépassent rarement 1,25 mm de diamètre. On commence par un concassage primaire suivi d’un concassage secondaire. Puis on continue par un broyage humide dans des broyeurs à boulets ou à barres. On obtient ainsi une pâte qui est soumise à la flottation . Celle-ci consiste à ajouter des réactifs à la pâte, qui forme des mousses sous l’action de l’air injecté. Un agent collecteur est ajouté, qui permet aux sulfures de s’attacher aux bulles. Les mousses débordent des cellules de flottation, sont épaissies, filtrées et séchées. La poudre ainsi obtenue est appelée concentré .
Traitements métallurgiques
Minerais sulfurés
On commence par agglomérer le concentré pulvérulent grâce à l’élévation de la température due à une oxydation partielle des sulfures avec combustion du soufre. Cette opération s’effectue avec un appareil Dwight-Lloyd, sorte de grille mobile à température contrôlée.
La métallurgie des minerais sulfurés est fondée sur l’affinité du cuivre pour le soufre et sur l’isolement, grâce à leur point de fusion relativement bas, des sulfures complexes de cuivre et de fer. Ces sulfures, appelés mattes, sont traités à l’état fondu, le fer étant séparé sous forme de silicates. Il reste du sulfure de cuivre que l’on oxyde pour obtenir le métal.
La production des mattes se fait dans des waterjackets , hauts fourneaux à double paroi refroidie à l’eau. Le concentré aggloméré mêlé à du coke est introduit par le haut de l’appareil; on y ajoute des fondants. De l’air est insufflé à la base. Les sulfures lourds de cuivre et de fer se rassemblent dans le creuset du waterjacket. La scorie liquide surnage et peut être évacuée facilement.
Les fours à réverbère permettent d’obtenir les mattes en évitant le grillage préalable. Le four électrique est réservé à des quantités de minerais moyennes (de 500 à 700 t par jour) et n’est intéressant que lorsque le prix de l’électricité est bas; il est avantageux lorsque la charge du four contient beaucoup de magnétite.
Après production des mattes, il faut opérer un convertissage entre 1 220 et 1 350 0C dans un four rotatif où l’on injecte de l’air. Les réactions caractéristiques qui s’y opèrent sont les suivantes:
– réaction de l’oxygène et du sulfure de fer:
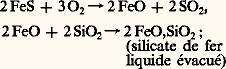
– réaction de l’oxygène et du sulfure de cuivre:

Ces deux dernières réactions se produisent simultanément et donnent:

L’opération dure quatre heures et produit 60 tonnes de cuivre. Le métal est transporté dans des fours où il est coulé en lingots de 150 kilogrammes. On se trouve en présence d’un cuivre relativement impur (99 p. 100), appelé blister (du mot anglais signifiant «cloque», caractérisant son état de surface). Après un autre processus d’affinage, le cuivre est coulé sous forme d’anodes pour être traité électrolytiquement.
Minerais oxydés
Les minerais riches peuvent être réduits directement au waterjacket. Les minerais ordinaires sont traités au four réverbère. Dans les deux cas, le produit obtenu est un cuivre blister. À partir de ce stade, le blister, qu’il provienne de minerais sulfurés ou oxydés, doit être raffiné.
Lorsque l’électricité est bon marché sur les lieux de production, on peut mettre en solution le minerai oxydé dans de l’acide sulfurique, la liqueur étant ensuite électrolysée sur des anodes en plomb:
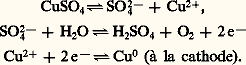
L’affinage thermique pratiqué sur des blisters ne contenant pas certaines impuretés peut donner un cuivre à haute conductivité électrique appelé «cuivre affiné thermique H. C.». Les quantités de cuivre ainsi affinées sont beaucoup plus faibles que celles qui sont traitées par électrolyse. L’affinage au feu doit être complété par un affinage électrolytique pour les variétés de cuivre blister provenant de minerais contenant des métaux précieux et des impuretés que l’on ne pourrait éliminer autrement (nickel, bismuth, sélénium, tellure). Le produit obtenu est appelé «cuivre électrolytique».
L’opération thermique consiste à souffler de l’air dans des fours réverbères. On oxyde ainsi partiellement le cuivre sous forme d’oxyde cuivrique qui réagit avec le sulfure résiduel:
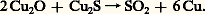
L’oxygène oxyde en même temps directement le soufre, le zinc, l’étain et le fer. Ces oxydes sont éliminés à l’aide de fondants siliceux. Le plomb, l’arsenic et l’antimoine le sont par addition de carbonate de sodium.
Le cuivre pur restant en fin d’opération est suroxydé. Pour ramener la teneur en oxygène à 0,04 p. 100, teneur normale du cuivre électrolytique, on pratique le perchage . Cette opération consiste à plonger des troncs d’arbres dans le bain de métal liquide. La combustion brutale du bois dégage des gaz réducteurs. Le cuivre est ensuite coulé sous forme d’anodes, plaques à «oreilles» destinées à être traitées électrolytiquement. Ce procédé n’est presque plus utilisé.
Affinage électrolytique
L’électrolyse s’effectue en quatorze jours. Elle permet de déposer sur des feuilles de cuivre minces, appelées cathodes de départ, des cathodes de cuivre pur (99,95 p. 100 au moins). Les impuretés sont soigneusement recueillies, car elles contiennent des métaux précieux qui font l’objet de récupérations ultérieures. L’électrolyte est du sulfate de cuivre additionné d’acide sulfurique et de divers agents. Les cathodes, après lavage, sont refondues et subissent à nouveau le cycle oxydation-perchage. Les cathodes sont soit livrées aux producteurs de «fil machine» en vue de la coulée continue de fil destiné aux usages électriques, soit coulées sous forme de plateaux destinés aux produits laminés, de billettes destinées aux barres, tubes et profilés ou de lingots pour l’élaboration des alliages de fonderie.
Les plateaux et billettes peuvent, par ajouts de phosphore, être livrés dans la qualité dite «désoxydée», nécessaire pour certaines applications non électriques; cette qualité de cuivre peut être chauffée en atmosphère réductrice.
Transformation
Dans le cas du cuivre pur, on part des cathodes ou des produits bruts: barres à fils, plateaux, billettes venant des raffineries ou élaborés sur place à partir de blisters auxquels on ajoute des déchets et chutes de fabrication.
Dans le cas d’alliages, et particulièrement pour les laitons, les transformateurs commencent par fondre des charges soigneusement dosées contenant des lingots de cuivre et de zinc et des chutes triées: tournures, vieux métaux, etc. Cette opération s’effectue le plus souvent au four électrique à induction.
La coulée est continue ou semi-continue. Les produits de coulée, après inspection et écroûtage, sont réchauffés au four avant transformation.
Produits tréfilés
Le procédé consistant à laminer à chaud des wire-bars , ou barres à fils, a disparu. Il a été remplacé par des procédés permettant l’obtention directe de fil machine, produit destiné à alimenter le tréfilage.
La coulée continue suivant diverses variantes (procédés South-wire , Contirod , Krupp ) consiste à couler directement le cuivre provenant de la fusion contrôlée de cathodes dans une goulotte mobile où il se solidifie. Encore chaud et malléable, le produit, de section trapézoïdale, passe dans une série de laminoirs qui lui donne la section circulaire de diamètre convenable. Le fil machine ainsi produit est décapé et conditionné en bottes de 5 tonnes environ.
Citons également le procédé de dip-forming (ou par accrescence), dans lequel un fil de départ est tiré à travers un bain de cuivre liquide à l’abri de l’air. Ce fil grossit et il est ensuite laminé.
La coulée continue convient à d’importantes unités de production – de 100 000 à 150 000 tonnes par an – alors que le dip-forming paraît mieux adapté à de petites productions – de l’ordre de 20 000 à 40 000 tonnes par an. Le fil est ensuite tréfilé sur des machines avec filière de tailles décroissantes. Il est ainsi possible d’arriver à des fils d’un diamètre de quelques centièmes de millimètre. Des recuits intermédiaires sont nécessaires lorsque le métal s’écrouit.
Les fils sont ensuite traités (émaillés, isolés, câblés...) pour satisfaire aux besoins de l’industrie électrique.
Produits laminés
Les plateaux réchauffés au four sont tout d’abord dégrossis à chaud. Les ébauches obtenues sont écroûtées à la fraiseuse, puis laminées à froid. Les laminoirs de finition sont le plus souvent des quartos . Les bandes sont recuites en cours de laminage, et décapées lorsque le recuit n’a pas été conduit sous atmosphère protectrice. Les bandes sont ensuite soit coupées à longueur pour faire des tôles, soit refendues pour obtenir des largeurs plus faibles et des rubans. Les produits plats ultra-minces, d’épaisseur inférieure à 70 micromètres, employés dans la fabrication des circuits imprimés, sont le plus souvent obtenus par électrodéposition directe et non par laminage.
Les barres et profilés sont obtenus à partir d’une billette réchauffée au four et filée à la presse à travers une filière. L’ébauche obtenue est ensuite reprise à froid sur des bancs à étirer pour obtenir l’écrouissage voulu et les dimensions requises. Là encore, des recuits et décapages intermédiaires sont nécessaires.
Les tubes sont filés à la presse à partir de billettes préalablement réchauffées – dans ce cas, la billette est percée soit avant, soit au moment du filage – ou obtenus sur laminoirs perceurs (type Mannesmann ou Stiefel). L’ébauche creuse est ensuite décapée et étirée sur bancs horizontaux, sur tambour (bull-block ) ou sur rotubloc . Les opérations de transformation du demi-produit se mécanisent de plus en plus.
Les alliages cuivreux peuvent être moulés suivant la plupart des procédés de fonderie: en cire perdue, en sable, en coquille par gravité ou sous pression. On notera simplement que le cuivre pur, par suite de sa grande affinité pour les gaz, est difficile à mouler sans addition de désoxydants, qui peuvent perturber notablement ses propriétés électriques.
Le moulage sous pression des laitons présente des difficultés par suite de l’usure assez rapide des outillages, des coquilles en molybdène presque pur (TZM: titane-zirconium-molybdène) donnant cependant d’excellents résultats.
Mise en œuvre
Le cuivre et ses alliages se prêtent pratiquement à toutes les formes connues de mise en œuvre: usinage, estampage, matriçage, emboutissage, filage par choc, soudage et brasage.
Le laiton est par excellence l’alliage de décolletage ; on lui ajoute du plomb à raison de 1 à 3 p. 100, ce qui a pour effet de faciliter la rupture du copeau. Le cuivre pur s’usine assez difficilement; l’addition de tellure, de soufre ou de plomb facilite les opérations d’usinage. Les bronzes s’usinent bien, les cupro-aluminiums, maillechorts et cupronickels possèdent une aptitude à l’usinage variable selon les compositions.
Le cuivre et ses alliages peuvent être frappés à froid, les laitons riches en cuivre s’y prêtant mieux que les laitons riches en zinc.
Les alliages cuivreux se matricent à chaud avec facilité, particulièrement les laitons dits de matriçage (à 39 p. 100 de zinc et de 1 à 1,5 p. 100 de plomb). Les températures de matriçage varient avec les titres et se situent généralement aux environs de 750 0C.
Les alliages de cuivre sont aptes à l’emboutissage, un exemple caractéristique étant celui du laiton à 33 p. 100 de zinc. Les passes d’emboutissage sont entrecoupées de recuits suivis de décapage pour les déformations importantes.
Le cuivre très pur complètement recuit et les laitons se prêtent au filage par choc. Cette opération reste cependant plus difficile qu’avec l’aluminium.
Le cuivre et ses alliages sont soudables, se brasent bien (brasures à l’argent et au phosphore), se soudobrasent et sont particulièrement aptes au brasage tendre (brasage à l’étain).
Les hautes conductivités électrique et thermique du cuivre pur le rend difficile à souder par résistance et au chalumeau pour les fortes épaisseurs.
Les cuivres non désoxydés sont très sensibles à l’action des gaz réducteurs, et on doit en tenir compte lors de leur brasage ou de leur soudage au chalumeau ou au four en atmosphère réductrice.
Le cuivre et ses alliages peuvent être polis, vernis, revêtus électrolytiquement de nickel, chrome, argent, or, rhodium, étain, etc. Le cuivre peut lui-même, ainsi que le laiton ou le bronze, être déposé électrolytiquement sur d’autres métaux.
2. Propriétés du cuivre
Les propriétés du cuivre sont données dans le tableau 1.
Propriétés physiques et mécaniques
Le cuivre cristallise dans le système cubique à faces centrées (a = 0,366 nm). C’est, après l’argent, le meilleur conducteur de la chaleur et de l’électricité, mais cette conductivité est très affectée par les éventuelles impuretés (phosphore, arsenic et aluminium notamment). Les atomes étrangers déforment le réseau et rendent plus difficile le transport des électrons.
Les caractéristiques mécaniques du métal pur sont moyennes; elles le situent loin derrière l’acier, mais avant les métaux mous (zinc, plomb, étain). Sa dureté est 3 dans l’échelle de Mohs, la résistance à la traction est faible et l’allongement important. Les propriétés mécaniques du cuivre sont assez favorables à la mise en forme à chaud et à froid.
Le cuivre et ses alliages présentent cette intéressante particularité que leurs caractéristiques mécaniques s’améliorent lorsque la température baisse. De là leur utilisation comme matériaux cryotechniques dans l’industrie des gaz liquéfiés.
Du côté des hautes températures, au contraire, ils présentent deux inconvénients: la résistance à l’oxydation décroît avec la température et les caractéristiques mécaniques diminuent dès 200 0C pour le cuivre pur. Les cupronickels et les cupro-aluminiums sont, parmi les alliages de cuivre, ceux qui résistent le mieux aux températures élevées. Pour ces alliages, la température limite est de l’ordre de 400 à 500 0C selon le temps qu’ils demeurent à ces températures. Lorsqu’il faut associer résistance à la température et conductivité électrique, par exemple, on peut utiliser des matériaux composites.
Propriétés chimiques
Le cuivre précède l’argent et l’or dans le sous-groupe b de la première colonne du tableau périodique des éléments. Neuvième des dix éléments de transition compris entre le calcium et le gallium, il est le premier à posséder une sous-couche 3 d complète. L’arrangement des électrons implique que le cuivre est normalement monovalent, et les sels cuivreux ressemblent en effet aux sels d’argent, auxquels ils sont souvent mêlés dans la nature. L’oxyde, le sulfure et les halogénures cuivreux ont une structure covalente prédominante. Ils cristallisent dans le système cubique du type de celui de la blende. Les halogénures sont facilement fusibles et sont semi-conducteurs. L’ion Cu+ est incolore et diamagnétique. En raison de son rayon important (0,091 nm), il ne donne pas d’hydrates et ses complexes sont peu stables. D’une façon générale, les sels cuivreux sont instables en solution en raison de l’équilibre:
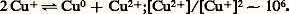
Les sels cuivriques anhydres cristallisés sont diversement colorés, mais la solution ammoniacale d’un sel cuivrique est toujours d’un beau bleu foncé, coloration caractéristique des ions [Cu (NH3)n ]2+; les hydrates ont une couleur bleue ou verte. Très stables, les complexes cuivriques (hydrates, ammines) sont tous paramagnétiques lorsqu’ils ont un électron célibataire et ont une structure dsp 2.
Métal noble, le cuivre, à l’inverse du fer, du zinc et du plomb, ne déplace pas l’hydrogène de ses solutions, et n’est donc pas soluble dans les hydracides. Il est soluble, en revanche, dans les acides oxydants (acide nitrique, acide sulfurique concentré et chaud). L’ammoniaque le dissout également en donnant une solution bleue connue sous le nom de « liqueur de Schweitzer ».
Le cuivre résiste bien à la corrosion atmosphérique et marine; une longue exposition entraîne la formation d’une fine couche de carbonate basique d’un beau vert. C’est la patine de certains toits.
Propriétés biochimiques
Le cuivre est, comme le fer, un élément indispensable à de nombreux processus vitaux. Il est le coenzyme de nombreuses métalloprotéines comme l’acide ascorbique oxydase et la tyrosinase. Mais son rôle principal est la stimulation de la synthèse de l’hémoglobine.
Ce rôle biologique du cuivre est probablement dû à la solidité des chélates qu’il forme avec les substances biologiques actives et à ses propriétés catalytiques intrinsèques.
Ses propriétés oxydoréductrices expliquent que les cupro-enzymes interviennent dans la chaîne respiratoire (au niveau de la cytochrome-oxydase probablement).
Les aliments contiennent naturellement du cuivre en quantité suffisante aux besoins de l’être humain; le corps en contient environ 12 milligrammes par kilogramme.
L’eau potable peut contenir du cuivre; au-dessus de 1,5 mg/l, certaines personnes particulièrement sensibles peuvent constater un goût. À très faibles teneurs, les sels de cuivre présentent une saveur désagréable très marquée rendant impossible l’ingestion involontaire de quantités toxiques.
Si le cuivre joue un rôle bénéfique vis-à-vis des organismes supérieurs, son comportement est totalement différent vis-à-vis des formes de vie inférieures; c’est le métal bactéricide le plus actif: un gramme de cuivre peut détruire jusqu’à 5 000 grammes de dangereux micro-organismes comme les colibacilles ou les staphylocoques dorés.
L’emploi de matériaux cuivreux dans les cliniques et dans tous les édifices publics améliorerait la prophylaxie des infections.
Composés du cuivre
Le cuivre est moins utilisé sous forme de sel que sous forme métallique. Le métal à l’état pur présente des propriétés de catalyseur mises à profit par certaines industries, la pétroléochimie notamment.
Le plus employé des sels de cuivre est le sulfate, qui est à la base de la bouillie bordelaise, dans laquelle l’acidité du sulfate est neutralisée par de la chaux. Ce produit est employé en agriculture et en viticulture. On lui substitue parfois la bouillie bourguignonne, dans laquelle la chaux est remplacée par du carbonate de calcium. L’oxychlorure de cuivre associé à d’autres produits de synthèse tend à se substituer au sulfate.
Il semble que l’effet du cuivre soit non seulement fongicide, mais aussi nécessaire à la croissance de nombreuses plantes. Cela est mis en évidence par le fait que des sols stériles, par suite de carence en cuivre, ont pu être mis en production par l’addition d’engrais contenant du cuivre. Les carences en cuivre peuvent également se traduire dans les prés par le dépérissement des animaux qui y pâturent. L’addition de quelques kilogrammes de sulfate de cuivre à l’hectare y remédie parfaitement.
Les sels de cuivre servent en outre à protéger les bois contre la pourriture, à protéger les semences, à l’enduction de certains tissus, à fabriquer des peintures antifouling retardant la fixation d’organismes marins sur les coques de navires. Ils sont très utilisés dans les bains d’électrolyse pour cuivrage d’aciers ou d’autres métaux.
Une application peu connue des sels de cuivre consiste dans l’utilisation de sulfate de cuivre comme additif aux aliments des porcs. L’addition de 250 p.p.m. à ces aliments entraîne une augmentation plus rapide du poids de l’animal, et plusieurs centaines de tonnes sont utilisées annuellement en France à cet effet. Le cuivre est trop souvent considéré comme un métal toxique. En fait, il n’existe pas de maladie professionnelle du cuivre. Nécessaire à la vie, ce métal semble jouer un rôle important dans la formation de l’hémoglobine du sang. Le docteur Kohei Toyokawa, de la faculté de médecine de T 拏ky 拏, a pu mettre en évidence l’influence favorable du cuivre sur le développement de l’animal.
3. Alliages de cuivre
Laitons
Les laitons sont des alliages à base de cuivre et de zinc ; ils renferment de 5 à 45 p. 100 de zinc et, éventuellement, divers autres éléments en faibles proportions destinés à améliorer certaines propriétés.
Selon leur composition, les laitons peuvent être soit moulés, soit travaillés à chaud ou à froid. Ils sont utilisés sous forme de tôles, de bandes droites ou roulées, de barres, de tubes, de fils, et présentent une remarquable aptitude à la mise en œuvre, supérieure à celle de la plupart des autres alliages industriels.
La teinte agréable des laitons, variant du rose au jaune selon la teneur en zinc, leur bonne résistance à la corrosion et leur aptitude aux traitements de surface permettent de réaliser économiquement des objets de belle présentation, d’un usage durable et d’un entretien facile.
Laitons simples
Ce sont des alliages binaires de cuivre et de zinc. À la température ordinaire, les laitons sont constitués d’une seule phase ( 見) jusqu’à 33 p. 100 de zinc et d’un mélange de deux phases ( 見 + 廓 ) de 33 à 46 p. 100. La phase 見, cubique à faces centrées, est malléable à chaud et à froid; elle permet des déformations importantes par laminage, emboutissage, etc.
La phase 廓 est dure et fragile; lorsque sa proportion croît, l’alliage devient plus usinable mais moins facilement déformable à froid. Au chauffage, la phase 廓 est remplacée par une phase cubique centrée beaucoup plus malléable (phase 廓).
Autres laitons
L’industrie emploie surtout des laitons au plomb, dits laitons de « décolletage », qui présentent une aptitude à l’usinage supérieure à celle de tous les autres alliages industriels. Pratiquement insoluble dans les laitons, le plomb (environ 2 p. 100) y est disséminé en fins globules qui provoquent la fragmentation des copeaux. Il joue également le rôle de lubrifiant en raison de son bas point de fusion.
Les laitons dits spéciaux résultent de l’incorporation d’un ou plusieurs éléments dont les plus employés sont: l’étain, l’aluminium, le manganèse, le nickel, le fer et le silicium. Ils se répartissent dans les phases 見 et 廓 dont ils modifient les propriétés physico-chimiques ainsi que les proportions relatives.
Bronzes
Les bronzes sont essentiellement des alliages de cuivre et d’étain, bien que l’on parle parfois de bronze d’aluminium ou de bronze au béryllium.
La teneur en étain des alliages industriels est comprise entre 3 et 20 p. 100. Aux teneurs plus élevées, les bronzes deviennent de plus en plus fragiles, et ils sont alors réservés à des emplois très particuliers, comme le bronze à cloche qui renferme de 20 à 25 p. 100 d’étain.
En raison de leur excellente aptitude au moulage, les bronzes sont surtout des alliages de fonderie.
Bronzes binaires
Leur diagramme d’équilibre montre l’existence de plusieurs phases. La phase 見, cubique à faces centrées, est la phase riche en cuivre. Son domaine s’étend jusqu’à environ 15 p. 100 d’étain. Elle est malléable à chaud et à froid. La phase 嗀 est une phase cubique dure et fragile; c’est elle qui donne aux cloches leur sonorité. Au fur et à mesure que croît la teneur en étain, la phase 嗀 apparaît en quantité croissante sous une forme associée avec la phase 見 dans un eutectoïde 見 + 嗀. Les caractéristiques mécaniques des bronzes dépendent principalement de la teneur en composé 嗀.
Bronzes complexes
Les principaux éléments d’addition sont le phosphore, le zinc et le plomb.
Le phosphore, sous la forme de phosphure de cuivre, est utilisé pour désoxyder les bronzes, qui en renferment donc toujours un peu. À des teneurs plus élevées (de 0,1 à 0,2 p. 100), il forme avec le cuivre un composé Cu3P, dur et fragile, qui augmente la dureté et surtout améliore les qualités de frottement.
L’incorporation de 4 à 5 p. 100 de zinc diminue la proportion de composé 嗀 et, par suite, augmente la malléabilité des bronzes tandis qu’elle diminue leurs qualités de frottement. Le plomb joue dans les bronzes le même rôle que dans les laitons: il améliore l’aptitude à l’usinage et l’étanchéité des pièces moulées.
Ces différentes sortes de bronzes peuvent être utilisées comme métal antifriction dans les coussinets. La phase 嗀, dure, supporte l’arbre de transmission en acier sans former avec lui d’alliage, tandis que la phase 見, plus tendre, fait apparaître en s’usant des microcavités qui sont comblées par le lubrifiant.
Autres alliages
Le nombre des alliages de cuivre dépasse de très loin celui des autres alliages non ferreux. Les principaux éléments d’addition sont, avec le zinc et l’étain, l’aluminium, le nickel, le plomb et le manganèse.
Les cupro-aluminiums constituent toute une famille d’alliages, simples ou pouvant comporter des additions de nickel, fer ou manganèse. En règle générale, ces alliages, d’une belle couleur or, sont très résistants à la corrosion par de nombreux acides et par l’eau de mer, d’où leur emploi en génie maritime.
Outre la même excellente résistance à la corrosion, les cupronickels ont de bonnes propriétés mécaniques. Le nickel et le cuivre étant complètement miscibles à l’état solide, la composition de ces alliages n’est pas fixe. L’alliage renfermant 20 p. 100 de nickel est l’un des alliages commerciaux les plus ductiles. L’addition de certains éléments (silicium, aluminium, chrome) rend possible un durcissement structural améliorant encore les propriétés mécaniques.
Les maillechorts sont des alliages ternaires renfermant de 20 à 28 p. 100 de zinc et de 9 à 26 p. 100 de nickel. Leur couleur varie du jaune pâle au blanc. Ils sont malléables et plus résistants mécaniquement que les laitons. Ils peuvent être chromés, nickelés et argentés. Leurs applications vont du couvert en métal argenté aux clefs plates, en passant par les pièces et ressorts de contact utilisés en téléphonie.
Tous ces alliages ont des propriétés qui, pour intéressantes qu’elles soient, ne suffisent pas pour certaines applications. On a donc mis au point des cuivres dits faiblement alliés.
Cuivres faiblement alliés
Renfermant généralement moins de 1 p. 100 d’éléments d’addition, leurs caractéristiques mécaniques sont supérieures à celles du cuivre pur et ils conservent des caractéristiques électriques élevées.
Les principaux sont: le cuivre à l’argent (de 0,03 à 0,10 p. 100 d’Ag), dont les caractéristiques mécaniques sont conservées à une température plus élevée de 100 0C que celle du cuivre pur; le cuivre au cadmium (de 0,7 à 1 p. 100 de Cd), dont la conductivité atteint 88 p. 100 de celle du cuivre pur pour une résistance mécanique plus élevée; le cuivre au tellure (de 0,5 à 0,9 p. 100 de Te), cuivre de décolletage dont la conductivité atteint 98 p. 100 de celle du cuivre; le cuivre au chrome (de 0,5 à 0,9 p. 100 de Cr) est un alliage dit à «durcissement structural»; ses caractéristiques sont obtenues par un traitement thermique (trempe + revenu); elles dépassent de beaucoup celles du cuivre pur et sont conservées jusqu’à 500 0C; sa conductivité électrique est de l’ordre de 80 p. 100 de celle du cuivre; le cuivre au béryllium (de 1,8 à 2 p. 100 de Be), alliage à durcissement structural qui possède des caractéristiques mécaniques remarquables équivalentes à celles des aciers à outils; sa conductivité électrique atteint environ 25 p. 100 de celle du cuivre pur.
4. Économie du cuivre
Géographie
Les gisements de cuivre sont pour la plupart situés dans l’hémisphère Sud, alors que les consommateurs sont en majorité dans l’autre hémisphère. Les membres du Conseil intergouvernemental des pays exportateurs de cuivre (C.I.P.E.C.), c’est-à-dire le Chili, le Pérou, le Zaïre, la Zambie, ainsi que les pays associés au C.I.P.E.C., c’est-à-dire l’Australie, l’Indonésie, la Papouasie-NouvelleGuinée, contribuent pour 40 p. 100 à la production mondiale et pour plus de 50 p. 100 à celle du monde occidental. Parmi les gros producteurs miniers, les États-Unis, la C.E.I. et le Canada font partie des premiers consommateurs.
Les ressources en cuivre des États-Unis, qu’il s’agisse de la production minière proprement dite ou des récupérations à partir de déchets, ne suffisent pas à couvrir les besoins du pays, qui consomme le double de sa production. En revanche, la C.E.I., qui considère le cuivre comme un métal stratégique dont l’emploi domestique est contrôlé, vit en économie fermée.
L’Europe des Douze consomme plus de cuivre que les États-Unis. Il faut remarquer la place exceptionnelle du Japon (troisième consommateur mondial et premier raffineur avec le Chili); l’Allemagne occupe le quatrième rang.
Les pays producteurs membres du C.I.P.E.C. recherchent une intégration plus poussée vers l’aval, ce qui revient à exporter de plus en plus de cuivre raffiné et de blister. Cette évolution ne se fera qu’en faisant décroître la part du Japon, de l’Allemagne et des États-Unis dans le raffinage. Elle se réalisera dans la mesure où les pays du C.I.P.E.C. pourront investir dans l’électrolyse et l’énergie électrique, ce qui est en bonne voie pour la Zambie, le Zaïre et le Chili, qui commencent à être industrialisés.
La situation géographique de ces pays, leur régime politique et social ont une influence sur l’approvisionnement en cuivre. Des grèves prolongées (Pérou, Chili) ou des bouleversements politiques ont des conséquences graves sur la production de «métal rouge». En dépit de situations politiques parfois difficiles, les approvisionnements n’ont, en pratique, pas trop souffert.
L’exploration et la prospection sont, certes, loin d’être achevées, et il est certain que l’on découvrira d’autres gisements. La limitation de la production de cuivre provient d’avantage des capacités de fonderie-raffinage que de celles des mines.
Il ne serait pas économique de transporter du minerai brut dont la teneur maximale ne dépasse pas 4 p. 100, et qui est le plus souvent beaucoup plus basse. On tend donc à développer le plus possible le traitement du minerai sur place.
Le tableau 2, qui donne la production de cuivre brut, la production et la consommation de cuivre raffiné, appelle les commentaires suivants.
La production de métal raffiné est toujours plus élevée (15 p. 100 en moyenne) que la production minière. Cela traduit l’importance considérable du raffinage des déchets, qui fournit un métal présentant les mêmes caractéristiques que le métal de première fusion, avec lequel il est confondu dans la pratique.
Si l’on tient compte du cuivre contenu dans les alliages faisant l’objet de recyclage, on arrive à plus du quart de la ressource en cuivre. Le déchet de cuivre va donc, plus que pour d’autres métaux, jouer un rôle prépondérant sur le marché, par suite des propriétés physiques du cuivre et de sa valeur intrinsèque.
Il existe un rapport entre l’activité du secteur de la récupération et le niveau des prix du cuivre raffiné.
Parmi les sociétés productrices de cuivre, les principales sont les suivantes: Codelco et Zaldivar (Chili), American Smelting and Refining Company (A.S.A.R.C.O.), Anaconda Co., Gecamines (Zaïre), Inco, Kennecott Copper Corporation (R.T.Z.), Phelps Dodge Corporation, Noranda, Z.C.C.M. (Zambie), le groupe Anglo-American Freeport Indonesia.
Structure de l’industrie
En dehors des États-Unis, les concentrations verticales sont rares dans l’industrie du cuivre. Dans le reste du monde, les sociétés productrices se sont souvent refusées à faire concurrence à leurs clients et se sont cantonnées dans l’élaboration et la vente de «formats bruts», barres à fils, plateaux, billettes, etc., aux utilisateurs. Certains pays non dotés de ressources minières (Belgique, Allemagne, Japon...) possèdent une puissante industrie du raffinage qui traite des cuivres ne pouvant être raffinés sur le lieu de production, ainsi que des déchets et des minerais européens.
Prix du cuivre
Les prix de revient du cuivre varient dans de très larges proportions suivant les mines: il dépend, en particulier, du coût de la main-d’œuvre.
Depuis fort longtemps, les producteurs de cuivre se sont efforcés d’assurer dans l’ensemble une certaine stabilité des cours. Cependant, à de nombreuses reprises, le jeu de l’offre et de la demande s’est trouvé faussé. D’où des fluctuations de cours parfois fort importantes qui ont contribué à donner du cuivre l’image d’une matière première faisant l’objet de spéculations.
On ne peut faire ici un historique complet. Quelques événements marquants méritent cependant d’être rappelés: l’accord Secrétan de 1887, tentative française de contrôle du marché du cuivre, a abouti à un krach retentissant; après la guerre de 1914-1918, les producteurs américains, non suivis par les autres pays, tentent de créer une association, Copper Exporters Inc., qui parvient à contrôler 86 p. 100 de la production, mais, par suite de la crise mondiale, on assiste à un effondrement des cours en 1931 (5 cents la livre, prix le plus bas jamais constaté); un Cartel international du cuivre est constitué en 1935; pendant la Seconde Guerre mondiale, le gouvernement américain fixe le prix du cuivre et verse aux mines à prix de revient élevé une indemnité compensatrice; après les hostilités, hauts et bas se succéderont: 436 livres la tonne en 1956, puis chute à 160 livres la tonne au début de 1958.
En 1958, le groupe Roan Selection Trust (à l’époque Rhodesian Selection Trust) prenait l’initiative de vendre son cuivre à prix fixe par contrats avec les utilisateurs importants. Les cours ayant monté, le R.S.T. se vit obligé de revenir au prix du marché.
Une autre tentative fut faite, par l’ensemble des producteurs, en 1962. Le cuivre était vendu à un «prix producteur» de 260 livres la tonne. Ce prix correspondit à celui du marché de Londres pendant un certain temps, jusqu’à l’apparition d’un déséquilibre statistique dû à un accroissement plus important que prévu de la consommation. Les utilisateurs européens, en fait, payaient un prix moyen représentant une péréquation entre le prix producteur et celui du marché de Londres. Les producteurs chiliens furent les premiers à augmenter le prix producteur, bientôt suivis par les autres producteurs. Il existe deux catégories de cours du cuivre: les prix du marché et les prix contractuels. Les marchés libres aux Bourses des métaux de Londres (London Metal Exchange) et de New York (New York Commodity Exchange, ou Comex) jouent un role décisif en matière de cotation. Londres sert de référence pour les contrats négociés hors des États-Unis et la London Metal Exchange traite la plus grande partie de l’offre mondiale du cuivre. Les entreprises américaines échangent le métal rouge à des prix légèrement supérieurs à ceux du Comex, plus stables.
Beaucoup de pays consommateurs font appel à des organismes nationaux qui achètent le cuivre à des prix contractuels ajustés sur le cours de la Bourse de Londres.
Facteurs influençant les cours
La ressource minière est abondante; on découvre de nouveaux gisements, et d’importantes augmentations de production sont prévues. L’augmentation de la productivité et les progrès de la technique ont permis d’exploiter économiquement des mines dont la teneur est basse. Ce facteur joue donc relativement peu.
Cependant, la production de cuivre, par sa nature même, n’est pas souple: on ne peut ajuster la production à la demande avec rapidité. Il s’écoule souvent six années entre la détermination d’un gisement et sa mise en exploitation. Une mine fermée pendant une période de sous-consommation ne peut être rouverte du jour au lendemain. Il est donc très important, mais très difficile, de prévoir la demande à venir avec autant d’exactitude que possible.
Les sous-produits des gisements de cuivre tels que l’or, l’argent, le cobalt, le molybdène ont pris une importance croissante. Dans certains cas et à certaines époques, les recettes en provenance des sous-produits étaient supérieures aux recettes du cuivre, ce qui a permis aux mines produisant de grandes quantités de sous-produits de poursuivre une exploitation rentable à des prix qui ne convenaient point aux mines dont les recettes des sous-produits étaient faibles.
La spéculation dans les marchés à terme de produits de base a considérablement augmenté dans les années 1970 et 1980. Il est indubitable que les hauts et les bas de l’activité des spéculateurs ont une énorme influence sur les cours du cuivre sur les marchés, en particulier pour les transactions à court terme.
Facteurs politiques et sociaux
Le cuivre constitue pour plusieurs des pays exportateurs, Chili, Pérou, Zaïre, Zambie, Papouasie – Nouvelle-Guinée et Philippines, une des principales ressources, voire la seule. Le prix du cuivre a, par exemple, une incidence directe sur le budget chilien. Les gouvernements de ces pays auront donc naturellement tendance à prélever sur le cuivre, richesse nationale, des taxes et redevances aussi élevées que possible. D’autre part, les syndicats ouvriers cherchent à tirer parti des périodes de cours élevés pour obtenir des avantages et augmentations de salaire. Ces facteurs constituent également un élément de hausse des cours.
Cependant, on sait qu’un prix trop élevé incite les utilisateurs à se tourner vers des produits de substitution et qu’à un certain niveau de nombreuses applications du cuivre pourraient être perdues au profit de l’aluminium, de l’acier inoxydable, des matières plastiques, etc. Un équilibre naturel tend ainsi à s’établir.
Pendant une période de vingt ans, jusqu’en 1983, le prix du cuivre était supérieur à celui de l’aluminium, parfois de 2,5 à 3 fois, et le cuivre a donc dû céder des parts de marché à ce métal, en particulier dans les domaines des fils et des câbles. Au cours de l’année 1983, le prix de l’aluminium a dépassé celui du cuivre; cette tendance ne s’est pas poursuivie. En 1992, le prix du cuivre dépassait légèrement celui de l’aluminium.
Autres facteurs
La technique évolue très rapidement. Telle utilisation traditionnelle du métal rouge peut décliner, telle autre au contraire augmenter. Par exemple, la miniaturisation des appareils électroniques amène une diminution de la consommation de certains fils; en revanche, le développement des emplois du gaz naturel conduit à un accroissement du nombre de chauffe-eau ou de chaudières de chauffage comportant du cuivre. Il est extrêmement difficile de prévoir à long terme l’influence des facteurs techniques.
L’augmentation de la population du globe, l’équipement de pays en voie de développement sont aussi des facteurs qui tendent à augmenter la demande en cuivre.
Situation actuelle
Le London Metal Exchange a été créé en 1882; on y cote, outre le cuivre, le plomb, l’étain, le zinc, l’argent, l’aluminium et le nickel. La confrontation de l’offre et de la demande conduit à formuler deux fois par jour une cotation qui est retenue comme base pour un grand nombre de contrats internationaux.
L’étroitesse relative des transactions physiques passées à Londres aboutit malheureusement à ce que des transactions portant sur de faibles tonnages servent de référence à des tonnages mondiaux beaucoup plus importants. Cependant, le London Metal Exchange est avant tout un «baromètre», qui traduit avec parfois un certain retard ou une certaine avance les positions respectives de l’offre et de la demande, en tenant compte de tous les éléments qui, directement ou indirectement, interviennent sur la tendance.
Les utilisateurs américains bénéficient d’un cours qui varie selon les producteurs, mais reste voisin des cotations du London Metal Exchange. En outre, le London Metal Exchange a une fonction d’arbitrage; par le jeu d’opérations simultanées sur le comptant et sur le terme, il permet de se couvrir contre les variations de cours.
Les grandes sociétés minières productrices de cuivre, bien loin de chercher à spéculer, recherchent plutôt un équilibre des cours à un niveau qui permette à la fois une rémunération raisonnable des investissements, un revenu substantiel pour le pays producteur, une provision pour la recherche de nouveaux gisements tout en constituant un frein à la substitution.
L’étude de la situation au cours des dernières années montre que l’équilibre entre offre et demande est très rarement atteint et se traduit par une légère baisse. Ce phénomène s’explique par une relative stabilité de la consommation mondiale. La solution du problème existe-t-elle? Passe-t-elle par un organisme international avec constitution de stocks tampons? L’avenir le dira.
La C.N.U.C.E.D. (Conférence des Nations unies sur le commerce et le développement) a tenu sous ses auspices dix-huit réunions dont l’objectif était de tenter d’atteindre un accord international pour le cuivre, analogue à ceux qui existent déjà pour l’étain, le café, le cacao et le sucre. Il est maintenant peu probable que l’on parvienne à la conclusion d’un tel accord dans un avenir proche.
Perspectives
L’industrie du cuivre dans le passé ne s’est jamais groupée. La concurrence internationale et surtout les lois antitrusts américaines s’y opposaient. Il en était résulté un retard certain en matière de recherche fondamentale ou appliquée. Aussi, les principaux producteurs de cuivre ont-ils créé une Association internationale de recherches pour le cuivre (I.N.C.R.A.), dont la mission consiste à étudier systématiquement les débouchés nouveaux pouvant s’offrir au cuivre sous toutes ses formes: alliages nouveaux à propriétés améliorées, appareillages poussés contenant des métaux cuivreux, éléments d’addition, sels de cuivre, produits chimiques, etc. Parallèlement, l’I.N.C.R.A., au moyen de recherches sous contrat effectuées dans des laboratoires du monde entier, s’efforce d’améliorer les techniques de production, de transformation et de mise en œuvre du métal.
En 1967, quatre grands producteurs, le Chili, le Pérou, le Zaïre et la Zambie, fondèrent le Conseil intergouvernemental des pays exportateurs de cuivre (C.I.P.E.C.). Quatre autres pays, l’Indonésie, l’Australie, la Papouasie – Nouvelle-Guinée et la Yousgoslavie se joignirent ensuite aux quatre membres fondateurs. Cette organisation, dont l’ensemble des membres représente la majeure partie du commerce mondial du cuivre, recueille des informations et constitue une tribune pour les échanges d’idées et la coordination de certaines politiques à suivre, comme la promotion du cuivre, qui s’effectue par l’octroi de contributions financières à des centres de promotion du cuivre, dont la plupart se situent dans des pays industrialisés.
Au cours des dernières années, plusieurs grandes compagnies pétrolières, en particulier en Amérique du Nord, ont pris le contrôle de divers producteurs de cuivre, cela dans une tentative de diversification. Les effets de ces influences extérieures sur l’avenir de l’industrie du cuivre ne sont pas encore évidents. Il se peut qu’ils permettent de ralentir le rythme auquel les producteurs à coûts élevés se voient contraints de réduire la production, face aux forces du marché.
L’industrie du cuivre dispose d’un système satisfaisant de collectes et de distribution de statistiques relatives à la production, à la consommation, aux prix et aux stocks; cependant, les applications finales, le rapport entre la consommation du cuivre, d’une part, et la croissance économique et la production industrielle, de l’autre, sont moins bien connus; il en est de même de l’évolution probable de ces variables.
Seule une meilleure connaissance des données statistiques et économiques réelles mondiales du marché du cuivre pourra permettre de prendre les mesures nécessaires, au niveau des gouvernements et des sociétés productrices, pour faire correspondre la production à la consommation et stabiliser les cours. La recherche systématique de débouchés nouveaux devrait permettre de compenser les pertes éventuelles dues à la substitution ou à l’évolution des techniques, une meilleure information des utilisateurs permettant, d’autre part, une utilisation judicieuse des propriétés du cuivre et de ses alliages.
La variation récente et favorable du prix du cuivre par rapport au prix de l’aluminium est un signe encourageant pour l’avenir.
cuivre [ kɥivr ] n. m.
• 1160; lat. °coprium, cuprium, class. cyprium, æs cyprium « bronze de Chypre »
I ♦ Corps simple (Cu; no at. 29; m. at. 63,54), métal rouge, très malléable et ductile, bon conducteur électrique. Minerais de cuivre. ⇒ cuprifère; azurite, chalcopyrite, chalcosine, covelline, cuprite, malachite. — Par ext. Cuivre gris : sulfure complexe à l'état natif. Cuivre jaune. ⇒ laiton. Alliages de cuivre. ⇒ cuproalliage; airain, argentan, bronze, chrysocale, constantan, laiton, maillechort, pacfung, tombac. — Oxydes de cuivre : oxyde cuivreux (Cu2O), oxyde cuivrique (CuO). Le cuivre s'oxyde à l'air. ⇒ vert-de-gris. Sulfate de cuivre (CuSO4) employé en viticulture dans la bouillie bordelaise. — Cuivre étamé. Casseroles en cuivre. « Les cuves et les appareils de cuivre rouge ont une couleur riche » (Chardonne). Clochette, cymbales en cuivre. Cuivre employé en bijouterie. ⇒ 2. clinquant, paillon. Gravure sur cuivre. ⇒ chalcographie.
II ♦ Plur. Objets en cuivre.
1 ♦ LES CUIVRES : ensemble d'instruments de cuisine, d'objets d'ornement en cuivre, en laiton (⇒ dinanderie) . Astiquer, faire briller les cuivres. Fam. Faire les cuivres. « Il nous enseigna l'emploi du tripoli pour le polissage des cuivres » (France).
2 ♦ Planches de cuivre gravées. Acheter les cuivres des illustrations d'un livre.
3 ♦ Ensemble des instruments à vent en cuivre employés dans l'orchestre. ⇒ 1. cor, saxhorn, saxophone, trombone, trompette. Orchestre de cuivres. ⇒ fanfare.
● cuivre nom masculin (latin populaire coprium, du latin classique aes cyprium, bronze de Chypre) Métal de couleur rouge-brun. (Élément chimique de symbole Cu.) Numéro atomique : 29 Masse atomique : 63,54 Masse volumique (à 20 °C) : 8,9 g°cm3 Température de fusion : 1 083,4 °C Objet, ustensile en cuivre : Nettoyer les cuivres. Planche de cuivre utilisée pour la gravure en taille-douce. ● cuivre (expressions) nom masculin (latin populaire coprium, du latin classique aes cyprium, bronze de Chypre) Cuivre noir, cuivre non purifié. Cuivre de Rosette, cuivre pur à l'état natif. Cuivre rouge, nom usuel du cuivre pur (par opposition au laiton, ou cuivre jaune). De cuivre, qui à la couleur rouge du cuivre.
cuivre
n. m.
rI./r élément métallique (symbole Cu) de numéro atomique Z = 29.
— Métal (Cu) usuel de couleur brun orangé. Fil de cuivre.
|| Cuivre jaune: laiton (par oppos. à cuivre rouge, cuivre pur).
rII./r Objet en cuivre.
d1./d Objet usuel ou d'ornement fait de cuivre ou de laiton. Fourbir, astiquer les cuivres.
d3./d TECH Planche gravée sur cuivre; gravure tirée de cette planche.
Encycl. Chim. - Le cuivre est un très bon conducteur de l'électricité (fabrication de fils électriques) et de la chaleur (ustensiles de cuisine). Il entre dans la composition de nombreux alliages: notam. bronzes et laitons.
⇒CUIVRE, subst. masc.
I.— [Le cuivre est envisagé comme métal]
A.— CHIM. MINÉRALE. Métal de couleur rouge-brun, ductile et malléable, bon conducteur de l'électricité, de symbole Cu. Synon. usuel cuivre rouge :
• 1. — Guitry, dit Bernard, c'est comme un fil de cuivre rouge. On sent qu'il rend 95 % de l'électricité qu'on lui communique.
RENARD, Journal, 1897, p. 443.
• 2. Nous traversons ensuite la région infernale des mines de cuivre du rio Tinto. C'est une suite d'immenses gradins circulaires taillés dans la montagne, et d'une pierre vert-de-gris ou marbrée comme l'ophite.
T'SERSTEVENS, L'Itinéraire espagnol, 1933, p. 165.
— [P. réf. à l'Antiq. et à l'alchimie médiév. qui mettaient le cuivre en relation avec Vénus, astre et déesse] Un long peigne de cuivre rouge, métal planétaire de la déesse (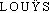 , Aphrodite, 1896, p. 114).
, Aphrodite, 1896, p. 114).
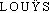 , Aphrodite, 1896, p. 114).
, Aphrodite, 1896, p. 114).SYNT. a) [Désignant divers états du cuivre ou de son extraction]. Cuivre natif. Cuivre noir. ,,Celui qui n'a pas encore été parfaitement purifié`` (Ac. 1798-1932). Cuivre pur, cuivre (de) rosette. ,,Celui qui a été entièrement purifié des autres métaux`` (LITTRÉ). Cuivre vierge. ,,Celui qui sort de la mine, qui n'a point été fondu`` (Ac. 1798-1932). Mines, minerai de cuivre. b) [Désignant des alliages à base de cuivre]. Cuivre blanc (vx). Alliage de cuivre, d'arsenic et de zinc ou étain. Cuivre jaune. ,,Alliage de cuivre et de zinc`` (Ac. 1798-1932). Synon. laiton. c) [Désignant des composés ou solutions à base de cuivre]. Oxyde de cuivre. Synon. vert-de-gris. Sels de cuivre, sulfate de cuivre. Synon. vitriol bleu. Eau de cuivre. Solution destinée à nettoyer les objets en cuivre. Eau de cuivre avec quoi dérouiller diverses garnitures de chasse (FLAUB., Mme Bovary, t. 2, 1857, p. 3). d) [Présentant le cuivre associé à un autre métal]. Le cuivre et l'acier, l'argent, le bronze, l'étain, le fer, le nickel, l'or, le plomb, le zinc; alliage de cuivre et d'étain.
B.— Ce métal en tant qu'il entre dans la fabrication ou la décoration de nombreux objets industriels ou domestiques.
1. Courant
a) Inanimé concr. + en/de cuivre
— En cuivre (compl. déterminatif à valeur prédicative). Les lustres à girandole de la paroisse, en cuivre jaune (GOZLAN, Notaire, 1836, p. 141).
— De cuivre (loc. à valeur adj.). Des tablettes en citronnier, à filets de cuivre (JOUY, Hermite, t. 1, 1811, p. 200). Dans l'ombre, une bassine de cuivre étincelait comme une face brûlante (MAURIAC, Génitrix, 1923, p. 382) :
• 3. Marianne, devant la porte, frottait la bassine de cuivre, trempant son chiffon mouillé dans le sable, et on voyait le beau dedans poli de la bassine devenir terne et gris, pendant qu'elle frottait toujours d'un mouvement en rond de tout son bras et de la tête. Puis, ayant été laver la bassine à grande eau, elle la rapportait, brillante comme un soleil.
RAMUZ, Aimé Pache, peintre vaudois, 1911, p. 293.
b) P. méton., gén. au plur.
— Domaine de l'écon. domestique. Ustensiles de cuisine, objets d'ornement en cuivre rouge ou jaune. La rangée de chaudrons, le tourne-broche, toute une artillerie de cuivres rouges (POURRAT, Gaspard, 1930, p. 76). Cf. aussi argent ex. 3 :
• 4. Les cuivres rutilaient : casseroles de toutes tailles, chaudrons, écumoires, bassines, bassinoires; ...
BEAUVOIR, Mémoires d'une jeune fille rangée, 1958, p. 77.
SYNT. Anneau, bague, baguette, balancier, barre, barreau, bassin, bijoux, boîte, boucle, bougeoir, bouilloire, boule, bouton, bracelet, casserole, chandelier, chaudron, clou, collier, croix, crucifix, dalle, disque, fermoir, fil, flambeau, fontaine, instrument, grelot, lampe, lit, médaille, marteau, miroir, monture, plaque, plat, plateau, poignée, pomme, pot, robinet, suspension, (clef à) tête de cuivre; tasse, tige, tringle, tube, tuyau, vase de cuivre; cerclé, doublé, incrusté de cuivre; cuivre argenté, brillant, ciselé, doré, étamé, poli, repoussé; astiquer, faire briller, frotter, nettoyer les cuivres. Faire les cuivres (fam.). Rendre leur éclat à des objets en cuivre. Se faire faire les cuivres (arg.) (SANDRY, CARRÈRE, Dict. arg. mod., 1953, p. 810; cf. briller, reluire).
— Domaine de la vie musicale. Instruments métalliques à vent de l'orchestre (généralement en laiton ou maillechort); p. méton., sonorités émises par ces instruments. Fracas des cuivres. Au beau milieu d'une symphonie de Beethoven, quand les cuivres déchirent l'oreille (FLAUB., Corresp., 1850, p. 148). La phrase qui prend aux cuivres gagne les bois et progressivement envahit les profondeurs de l'orchestre (CLAUDEL, G. odes, 1906, p. 241).
♦ P. métaph. Tout enfant on aime les cuivres sonores du Cid (BARRÈS, Cahiers, t. 9, 1911, p. 3).
♦ Au sing. collectif. La fanfare, à sa bouche appuyant les clairons, Fière, et faisant sonner la gloire dans le cuivre (HUGO, Légende, t. 5, 1877, p. 995).
2. P. méton., emplois spéc.
a) GRAV. Planche de cuivre gravée au burin en taille-douce; la gravure elle-même. Gravure sur cuivre, planche de cuivre. Un fac-similé sur cuivre de l'édition originale (BARRÈS, Voy. Sparte, 1906, p. 150) :
• 5. Il [Mabeuf] avait fait et publié une Flore des environs de Cauteretz avec planches coloriées, ouvrage assez estimé dont il possédait les cuivres et qu'il vendait lui-même.
HUGO, Les Misérables, t. 1, 1862, p. 820.
b) MONNAIE, vieilli. Pièce de monnaie en cuivre. Synon. billon. P. ext. Monnaie quelconque. S'il tombe du ciel un peu de cuivre, il va s'asseoir, le réfractaire, dans une de ces gargottes (VALLÈS, Réfract., 1865, p. 11).
II.— [Ce qui rappelle le cuivre]
A.— [Par sa couleur]
1. [De cuivre ou cuivre en emploi adj. inv.]
— De cuivre. Synon. cuivré. Le ciel de cuivre du couchant (HUGO, N.-D. Paris, 1832, p. 162). Quand vos cheveux de cuivre se déroulent sur vos épaules (CROS, Coffret santal, 1873, p. 126) :
• 6. À cinq heures et demie du matin, sous le rayon horizontal et la rosée, le blé jeune est d'un bleu incontestable, et rouge la terre ferrugineuse, et rose de cuivre les pruniers blancs.
COLETTE, La Maison de Claudine, 1922, p. 261.
— [Cuivre en appos. à un nom de couleur] Le rouge cuivre, couleur fort estimée au nord de l'Italie (NODIER, J. Sbogar, 1818, p. 88).
2. [En empl. subst.] Quelques gouttes de pluie sonnaient sur le cuivre doré des hêtres (ROLLAND, J.-Chr., Maison, 1909, p. 1084). Le cuivre des feuilles neuves (COLETTE, Duo, 1934, p. 12). Un bel adolescent (...) de poil ardent, entre cuivre et carotte (ARNOUX, Paris, 1939, p. 204).
B.— [Par sa sonorité] De cuivre. Synon. cuivré. Une voix de cuivre clamait par instants (PÉLADAN, Vice supr., 1884, p. 206) :
• 7. D'où part ce cri de cuivre [du coq] et l'écho au fond de notre poulailler de ce commandement du premier jour : Que la lumière soit!
CLAUDEL, Un Poète regarde la Croix, 1938, p. 39.
Prononc. et Orth. :[ ]. Ds Ac. 1694-1932. Étymol. et Hist. A. 1. Début XIIe s. agn. queivre (cf. beivre [< bibere]) (St Brendan, éd. E. C. Waters, 1416); 2. 1155 [ms. XIIIe s. agn.] quivre (WACE, Brut, éd. I. Arnold, 14648); 1165-76 cuivre [copie Guiot début XIIIe s.] (CH. DE TROYES, Cligès, éd. M. Roques, 2734); emplois métaphoriques a) 1823 « ustensile de cuisine » (BOISTE); b) 1845 grav. (BESCH.); c) 1832 plur. mus. (HUGO, N.-D. Paris, p. 83); emploi adj. 1818 (NODIER, J. Sbogar, p. 88); 3. ca 1160 [ms. A, fin XIIe-début XIIIe s.] coivre (Eneas, éd. J. Salverda de Grave2, 6432); 1160-74 [ms. XIIIe s., Normandie] id. (WACE, Rou, éd. A. J. Holden, 6452). B. 1288 [ms. A, traits picards] keuvre (Thèbes, éd. Constans, t. II, p. 107, 73), type en usage notamment en wallon, pic., fr.-prov. et occitan, v. FEW t. 2, p. 1614 b. B régulièrement issu du lat. impérial cyprum,
]. Ds Ac. 1694-1932. Étymol. et Hist. A. 1. Début XIIe s. agn. queivre (cf. beivre [< bibere]) (St Brendan, éd. E. C. Waters, 1416); 2. 1155 [ms. XIIIe s. agn.] quivre (WACE, Brut, éd. I. Arnold, 14648); 1165-76 cuivre [copie Guiot début XIIIe s.] (CH. DE TROYES, Cligès, éd. M. Roques, 2734); emplois métaphoriques a) 1823 « ustensile de cuisine » (BOISTE); b) 1845 grav. (BESCH.); c) 1832 plur. mus. (HUGO, N.-D. Paris, p. 83); emploi adj. 1818 (NODIER, J. Sbogar, p. 88); 3. ca 1160 [ms. A, fin XIIe-début XIIIe s.] coivre (Eneas, éd. J. Salverda de Grave2, 6432); 1160-74 [ms. XIIIe s., Normandie] id. (WACE, Rou, éd. A. J. Holden, 6452). B. 1288 [ms. A, traits picards] keuvre (Thèbes, éd. Constans, t. II, p. 107, 73), type en usage notamment en wallon, pic., fr.-prov. et occitan, v. FEW t. 2, p. 1614 b. B régulièrement issu du lat. impérial cyprum,  « cuivre » (FEW T. 2, p. 1615 a). Les formes rapportées en A sont généralement ramenées au lat. impérial cypruim,
« cuivre » (FEW T. 2, p. 1615 a). Les formes rapportées en A sont généralement ramenées au lat. impérial cypruim, 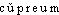 (aes), proprement « bronze de Chypre » [cf. PLINE, Nat., 7, 195 ds TLL s.v. Cypros, 797, 5] (MEYER-LÜBKE ds Z. rom. Philol., t. 36, 1912, p. 230; FEW, loc. cit.); cependant l'évolution phonét. demeure obsc. (cf. les tentatives d'explication de FOUCHÉ, pp. 403-405), v. F. DE LA CHAUSSÉE, Initiation à la phonét. hist., p. 127; il n'est pas impossible que le -i- s'explique par des confusions avec l'homon. a. fr. cuivre « carquois » (FEW t. 16, p. 429 b) qui présente la même alternance radicale. La forme isolée A 1 est peut-être une forme hyper-anglo-normande correspondant à l'a. fr. coivre. Fréq. abs. littér. :1 856. Fréq. rel. littér. :XIXe s. : a) 1 893, b) 3 850; XXe s. : a) 3 180, b) 2 301.
(aes), proprement « bronze de Chypre » [cf. PLINE, Nat., 7, 195 ds TLL s.v. Cypros, 797, 5] (MEYER-LÜBKE ds Z. rom. Philol., t. 36, 1912, p. 230; FEW, loc. cit.); cependant l'évolution phonét. demeure obsc. (cf. les tentatives d'explication de FOUCHÉ, pp. 403-405), v. F. DE LA CHAUSSÉE, Initiation à la phonét. hist., p. 127; il n'est pas impossible que le -i- s'explique par des confusions avec l'homon. a. fr. cuivre « carquois » (FEW t. 16, p. 429 b) qui présente la même alternance radicale. La forme isolée A 1 est peut-être une forme hyper-anglo-normande correspondant à l'a. fr. coivre. Fréq. abs. littér. :1 856. Fréq. rel. littér. :XIXe s. : a) 1 893, b) 3 850; XXe s. : a) 3 180, b) 2 301.
 ]. Ds Ac. 1694-1932. Étymol. et Hist. A. 1. Début XIIe s. agn. queivre (cf. beivre [< bibere]) (St Brendan, éd. E. C. Waters, 1416); 2. 1155 [ms. XIIIe s. agn.] quivre (WACE, Brut, éd. I. Arnold, 14648); 1165-76 cuivre [copie Guiot début XIIIe s.] (CH. DE TROYES, Cligès, éd. M. Roques, 2734); emplois métaphoriques a) 1823 « ustensile de cuisine » (BOISTE); b) 1845 grav. (BESCH.); c) 1832 plur. mus. (HUGO, N.-D. Paris, p. 83); emploi adj. 1818 (NODIER, J. Sbogar, p. 88); 3. ca 1160 [ms. A, fin XIIe-début XIIIe s.] coivre (Eneas, éd. J. Salverda de Grave2, 6432); 1160-74 [ms. XIIIe s., Normandie] id. (WACE, Rou, éd. A. J. Holden, 6452). B. 1288 [ms. A, traits picards] keuvre (Thèbes, éd. Constans, t. II, p. 107, 73), type en usage notamment en wallon, pic., fr.-prov. et occitan, v. FEW t. 2, p. 1614 b. B régulièrement issu du lat. impérial cyprum,
]. Ds Ac. 1694-1932. Étymol. et Hist. A. 1. Début XIIe s. agn. queivre (cf. beivre [< bibere]) (St Brendan, éd. E. C. Waters, 1416); 2. 1155 [ms. XIIIe s. agn.] quivre (WACE, Brut, éd. I. Arnold, 14648); 1165-76 cuivre [copie Guiot début XIIIe s.] (CH. DE TROYES, Cligès, éd. M. Roques, 2734); emplois métaphoriques a) 1823 « ustensile de cuisine » (BOISTE); b) 1845 grav. (BESCH.); c) 1832 plur. mus. (HUGO, N.-D. Paris, p. 83); emploi adj. 1818 (NODIER, J. Sbogar, p. 88); 3. ca 1160 [ms. A, fin XIIe-début XIIIe s.] coivre (Eneas, éd. J. Salverda de Grave2, 6432); 1160-74 [ms. XIIIe s., Normandie] id. (WACE, Rou, éd. A. J. Holden, 6452). B. 1288 [ms. A, traits picards] keuvre (Thèbes, éd. Constans, t. II, p. 107, 73), type en usage notamment en wallon, pic., fr.-prov. et occitan, v. FEW t. 2, p. 1614 b. B régulièrement issu du lat. impérial cyprum,  « cuivre » (FEW T. 2, p. 1615 a). Les formes rapportées en A sont généralement ramenées au lat. impérial cypruim,
« cuivre » (FEW T. 2, p. 1615 a). Les formes rapportées en A sont généralement ramenées au lat. impérial cypruim, 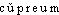 (aes), proprement « bronze de Chypre » [cf. PLINE, Nat., 7, 195 ds TLL s.v. Cypros, 797, 5] (MEYER-LÜBKE ds Z. rom. Philol., t. 36, 1912, p. 230; FEW, loc. cit.); cependant l'évolution phonét. demeure obsc. (cf. les tentatives d'explication de FOUCHÉ, pp. 403-405), v. F. DE LA CHAUSSÉE, Initiation à la phonét. hist., p. 127; il n'est pas impossible que le -i- s'explique par des confusions avec l'homon. a. fr. cuivre « carquois » (FEW t. 16, p. 429 b) qui présente la même alternance radicale. La forme isolée A 1 est peut-être une forme hyper-anglo-normande correspondant à l'a. fr. coivre. Fréq. abs. littér. :1 856. Fréq. rel. littér. :XIXe s. : a) 1 893, b) 3 850; XXe s. : a) 3 180, b) 2 301.
(aes), proprement « bronze de Chypre » [cf. PLINE, Nat., 7, 195 ds TLL s.v. Cypros, 797, 5] (MEYER-LÜBKE ds Z. rom. Philol., t. 36, 1912, p. 230; FEW, loc. cit.); cependant l'évolution phonét. demeure obsc. (cf. les tentatives d'explication de FOUCHÉ, pp. 403-405), v. F. DE LA CHAUSSÉE, Initiation à la phonét. hist., p. 127; il n'est pas impossible que le -i- s'explique par des confusions avec l'homon. a. fr. cuivre « carquois » (FEW t. 16, p. 429 b) qui présente la même alternance radicale. La forme isolée A 1 est peut-être une forme hyper-anglo-normande correspondant à l'a. fr. coivre. Fréq. abs. littér. :1 856. Fréq. rel. littér. :XIXe s. : a) 1 893, b) 3 850; XXe s. : a) 3 180, b) 2 301.DÉR. Cuivrique, adj., chim. [En parlant d'un composé] Qui contient du cuivre bivalent. Le liquide cuivrique potassé a permis de rechercher le sucre (BERNARD, Princ. méd. exp., 1878, p. 244). — [ ]. — 1re attest. 1834 (A.-J.-L. JOURDAN, Dict. (...) termes sc. nat., Paris); de cuivre, suff. -ique. — Fréq. abs. littér. : 1.
]. — 1re attest. 1834 (A.-J.-L. JOURDAN, Dict. (...) termes sc. nat., Paris); de cuivre, suff. -ique. — Fréq. abs. littér. : 1.
 ]. — 1re attest. 1834 (A.-J.-L. JOURDAN, Dict. (...) termes sc. nat., Paris); de cuivre, suff. -ique. — Fréq. abs. littér. : 1.
]. — 1re attest. 1834 (A.-J.-L. JOURDAN, Dict. (...) termes sc. nat., Paris); de cuivre, suff. -ique. — Fréq. abs. littér. : 1.BBG. — HUBSCHMID (J.). Afr. cuivre, dt. köcher : eine Wortfamilie hunnischen Ursprungs. In : Essais de Philol. mod. Paris, 1953, pp. 189-199.
cuivre [kɥivʀ] n. m.
ÉTYM. Déb. XIIe, queivre; quivre, coivre, jusque v. 1165; du lat. coprium, cuprium, lat. class. cyprium, ellipse d'aescuprium « bronze de Chypre ».
❖
1 Corps simple (symb. Cu); no at. 29; p. at. 63,54; métal rouge fusible à 1 083 °C, très malléable et ductile, bon conducteur électrique (dens. 8,96). ⇒ Chalco-, cupri-. || Cuivre rouge. ⇒ Rosette. || Minerais de cuivre. ⇒ Cuprifère; azurite, bournonite, chalcopyrite, chalcosine, chrysocolle (et préf. chryso-), cuprite, malachite. || Le cuivre est l'un des métaux les plus importants. || Cuivre vierge, non fondu, non raffiné. || Mine de cuivre. || Extraction, métallurgie du cuivre. || Fonderie de cuivre. || Traitement des minerais sulfurés de cuivre : grillage (en tas, en four à tablettes), fusion pour matte (en fours à cuve, en réverbères), convertissage en matte blanche, affinage. || Alliages de cuivre. ⇒ Airain, alfénide, argentan, bronze, chrysocale, constantan, laiton (ou cuivre jaune), maillechort, pacfung, potin, pyrope, tombac. || Cuivre blanc : alliage de cuivre, arsenic et étain. || Le bronze d'aluminium est un alliage de cuivre.
♦ Composés du cuivre (composés halogénés) : chlorure cuivreux (Cu2Cl2), chlorure cuivrique (CuCl2). || Oxydes de cuivre : oxyde cuivreux Cu2O (ou oxydule), oxyde cuivrique (CuO). || Sulfate de cuivre (CuSO4). || Sels de cuivre : sulfate (couperose bleue, vitriol bleu), azotate, carbonates (cuivre bleu) et hydrocarbonates (⇒ Azurite, malachite, vert-de-gris). || Sulfate de cuivre, employé en viticulture sous le nom de bouillie bordelaise. ⇒ Sulfatage. || Acétate de cuivre employé en bouillie anticryptogamique. ⇒ Verdet.
♦ Utilisations du cuivre. ⇒ Chaudronnerie, dinanderie, quincaillerie. || Cuivre embouti. || Cuivre repoussé. || Ustensiles de ou en cuivre. ⇒ Cuivré. || Batterie de cuisine, casseroles en cuivre. || Clou, cabochon en cuivre. || Clochette, cymbale en cuivre. || Récipient en cuivre servant au transport du lait. ⇒ 2. Canne. — Monnaie de cuivre. — Cuivre employé en bijouterie en faux. ⇒ Clinquant, paillon, oripeau. — Gravure sur cuivre. ⇒ Chalcographie. || Cliché typographique, galvanotype en cuivre. — Instruments de musique en cuivre (→ ci-dessous, 2., b. : les cuivres). — Emploi du cuivre par l'industrie électrique.
1 Qu'un joueur est heureux ! Sa poche est un trésor !
Sous ses heureuses mains le cuivre devient or.
J.-F. Regnard, le Joueur, III, 6.
2 J'étalerai mes baisers sans remords
Sur ton beau corps poli comme le cuivre.
Baudelaire, les Fleurs du mal, Épaves, IV, « Léthé ».
3 (…) vous y découvrirez, çà et là, quelques détails sur les alliages de cuivre rouge et d'étain fin (…)
Huysmans, Là-bas, IX, p. 130.
4 Sur une assise de briques, les cuves et les appareils de cuivre rouge, renflés en bulbes ou recourbés en col de cygne, ont une couleur riche de viscère rutilant, entre les murs noircis.
J. Chardonne, les Destinées sentimentales, I, III, p. 95.
♦ Âge du cuivre, précédant l'âge de bronze, marquant l'apparition des métaux (⇒ aussi Chalcolithique).
♦ En appos. || Rouge cuivre (⇒ Cuivré, cuivreux). — Le cuivre de qqch. : sa couleur cuivrée. || Le cuivre d'un sous-bois en automne.
➪ tableau Désignations de couleurs.
♦ Par ext. || Cuivre gris : sulfure complexe de cuivre à l'état natif. || Cuivre noir. || Cuivre jaune : laiton (alliage). || Cuivre vierge.
2 Généralt au plur. (Les cuivres). Objets en cuivre.
a (1823). Ensemble d'instruments de cuisine, d'objets d'ornement… en cuivre, en laiton (⇒ Dinanderie). || Astiquer, nettoyer, faire briller les cuivres. || Faire les cuivres (fam.). || Faire les cuivres avec de la pâte à cuivre, de l'eau de cuivre. || « Les cuivres luisants Au dos du comptoir » (→ Comptoir, cit. 0.2, Elskamp).
5 (…) nous enseigna doctement l'emploi du tripoli pour le polissage des cuivres.
France, le Crime de Sylvestre Bonnard, II, p. 396.
6 (…) un yacht étranger, en bonne place, à ras de quai, exhibait sans pudeur, ses cuivres, son électricité, son pont en bois des îles (…)
Colette, la Naissance du jour, p. 204.
7 (…) l'on voyait, sur le bahut, étinceler les plats et les grands cuivres rouges, polis religieusement par Sidonie.
H. Bosco, le Jardin d'Hyacinthe, Sidonie, III, p. 102.
b (1832). Ensemble des instruments à vent en cuivre employés dans l'orchestre. ⇒ Cor, saxhorn, trombone, trompette; clairon, cornet. || Orchestre de cuivres. ⇒ Fanfare. || Les cuivres de cet orchestre manquent de justesse. Au sing. collectif :
8 (…) Pour entendre un de ces concerts riches en cuivre,
Dont les soldats parfois inondent nos jardins (…)
Baudelaire, les Fleurs du mal, Tableaux parisiens, « Les petites vieilles », III.
9 Les cuivres et les roulements de tambour, les coups sourds de la grosse caisse rythmaient ses chansons et sa voix autoritaire qui bouleversait les soldats.
P. Mac Orlan, la Bandera, IX, p. 110.
10 Sigismond ne dérange personne en allant vers un rideau de vieux velours vert, derrière lequel se fait entendre un orchestre fort en cuivres.
A. Pieyre de Mandiargues, la Marge, p. 169-170.
c (1845). Planche de cuivre gravée; par métonymie, la gravure elle-même. || Acheter les cuivres des illustrations d'un livre. || De beaux cuivres.
11 Chez Villot vers trois heures et retouché le cuivre des Arabes d'Oran (…)
E. Delacroix, Journal, 13 juin 1847.
❖
DÉR. et COMP. Cuivrer, cuivrerie, cuivreux, cuivrique. Décuivrer.
Encyclopédie Universelle. 2012.